第一章物质结构元素周期律第一节元素周期表P6科学探究探究碱金属元素的金属性强弱的规律(1)实验步骤:①将一干燥的坩埚加热,同时取小块钾,擦干表面的煤油后,迅速投到热坩埚中,观察现象
再与钠与氧气的反应进行对比
②在培养皿中放入一些水,然后取黄豆粒大的钾,用滤纸吸干表面的煤油,投入培养皿中,观察现象
再与钠与水的反应对比
(2)实验现象:钾钠与氧气反应在热坩埚中能迅速燃烧并产生紫色火焰
在加热的条件下,钠能在空气中燃烧并产生黄色火焰与水反应浮在水面,融化成小球,四处游动,不时发出轻微爆炸,很快消失
浮在水面,融化成小球,四处游动,钠与水反应不能发生爆炸反应
(3)实验结论:钾比钠更容易与氧化合,钾比钠更容易与水反应,钾比钠金属性强
P9实验1-1探究卤族元素的非金属性强弱的规律(1)实验记录:实验现象化学方程式将少量氯水分别加入盛有NaBr溶液和KI溶液的试管中,用力振荡后加入少量四氯化碳,振荡、静置加入氯水后,NaBr溶液呈黄色;加入四氯化碳后,油层呈橙红色
加入氯水后,KI溶液呈黄褐色;加入四氯化碳2NaBr+Cl2=2NaCl+Br22KI+Cl2=2KCl+I2后,油层呈紫红色
将少量溴水加入盛有KI溶液的试管中,用力振荡后加入少量四氯化碳,振荡、静置加入溴水后,溶液呈黄褐色;加入四氯化碳后,油层呈紫红色
2KI+Br2=2KBr+I2(2)实验结论:较活泼的非金属单质能将较不活泼的非金属元素的阴离子从其盐溶液中置换出来
由此可以判断非金属性的强弱
P11习题1.1;1;Cs;Li;7;1;F;F
2.C3.C4.A5.(1)63Li73Li;(2)146C147N;(3)2311Na2412Mg
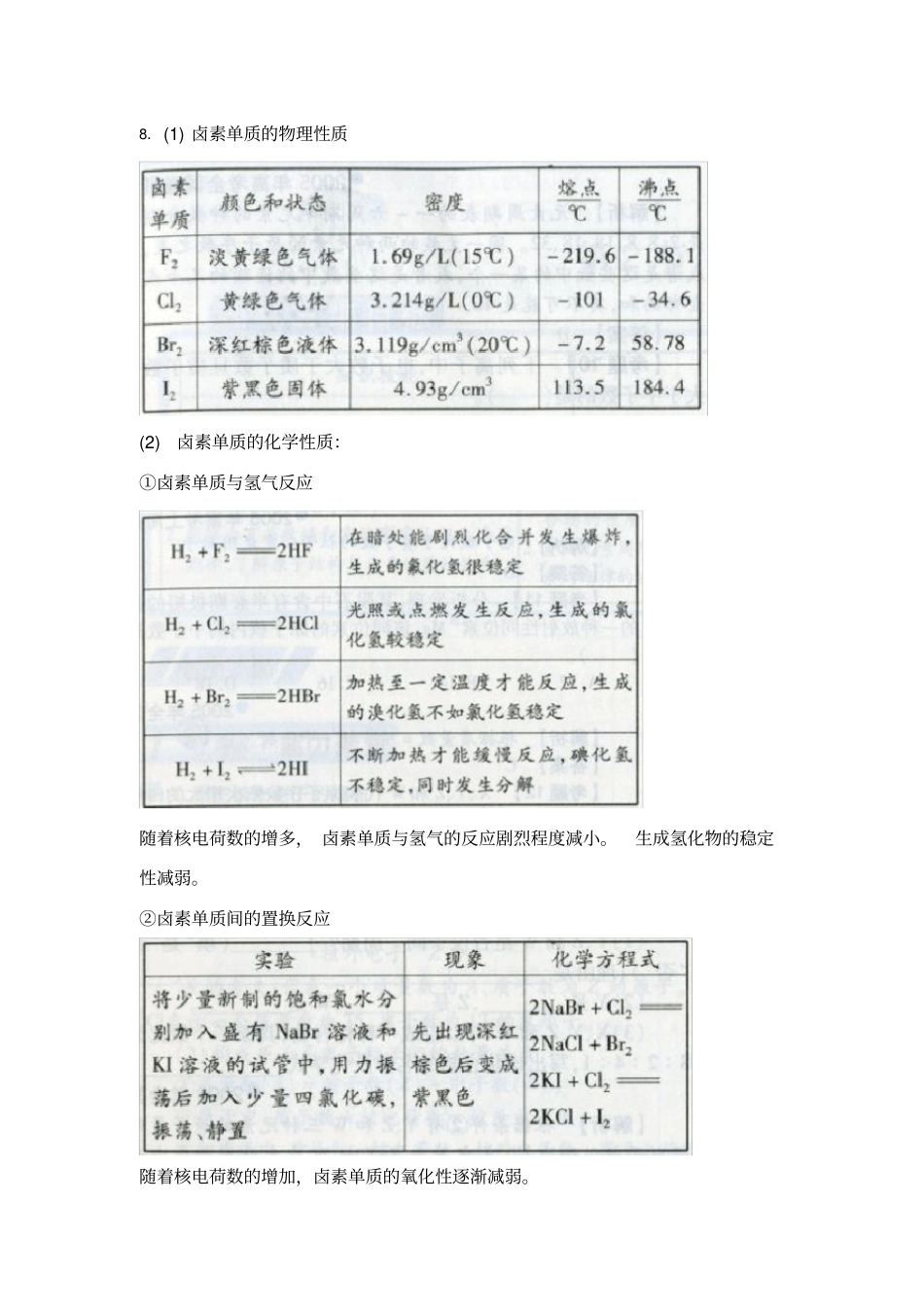
6.7.8.(1)卤素单质的物理性质(2)卤素单质的化学性质:①卤素单质与氢气反应随着核电荷数的增多,卤素单质与氢气的反应剧烈程度减小
生成氢化物的稳定性减弱
②卤素单质间