高考化学考点复习专题九氧、硫及其化合物和环境保护考点1硫及其氧化物硫的氢化物1
[2021江苏南京六校联考]下列制取SO2、验证其性质的装置(尾气处理装置已省略)和原理不能达到实验目的的是()2
[2021广东佛山南海区摸底测试]天然气是应用广泛的燃料,但含有少量H2S等气体
在酸性溶液中利用氧化亚铁硫杆菌可实现天然气的催化脱硫,其原理如图所示
下列说法不正确的是A
过程甲中发生反应的离子方程式为2Fe+H2SB
脱硫过程中O2间接氧化H2SC
该脱硫过程需要不断添加Fe2(SO4)3溶液D
过程乙中发生反应的离子方程式为4Fe+O2+4H2++3+()2Fe+S↓+2H2++4Fe+2H2O3+3
[2020四川成都摸底测试,11分]二氧化硫在生产和生活中有着广泛的用途
(1)SO2可用来制备定影剂Na2S2O3,反应的化学方程式为Na2CO3+2Na2S+4SO23Na2S2O3+CO2
请用单线桥表示该反应中的电子转移情况,还原剂与氧化剂的物质的量之比为
(2)用足量NaOH溶液吸收尾气中的SO2,反应的离子方程式为;吸收后的浓溶液可用图1所示装置再生循环脱硫,并制得硫酸,电极a的电极反应为,乙是
图1(3)可设计二氧化硫-空气质子交换膜燃料电池处理尾气中的二氧化硫,原理如图2所示
其能量转化的主要形式是,c电极是极,移动的离子及方向是
第1页共15页高考化学考点复习图24
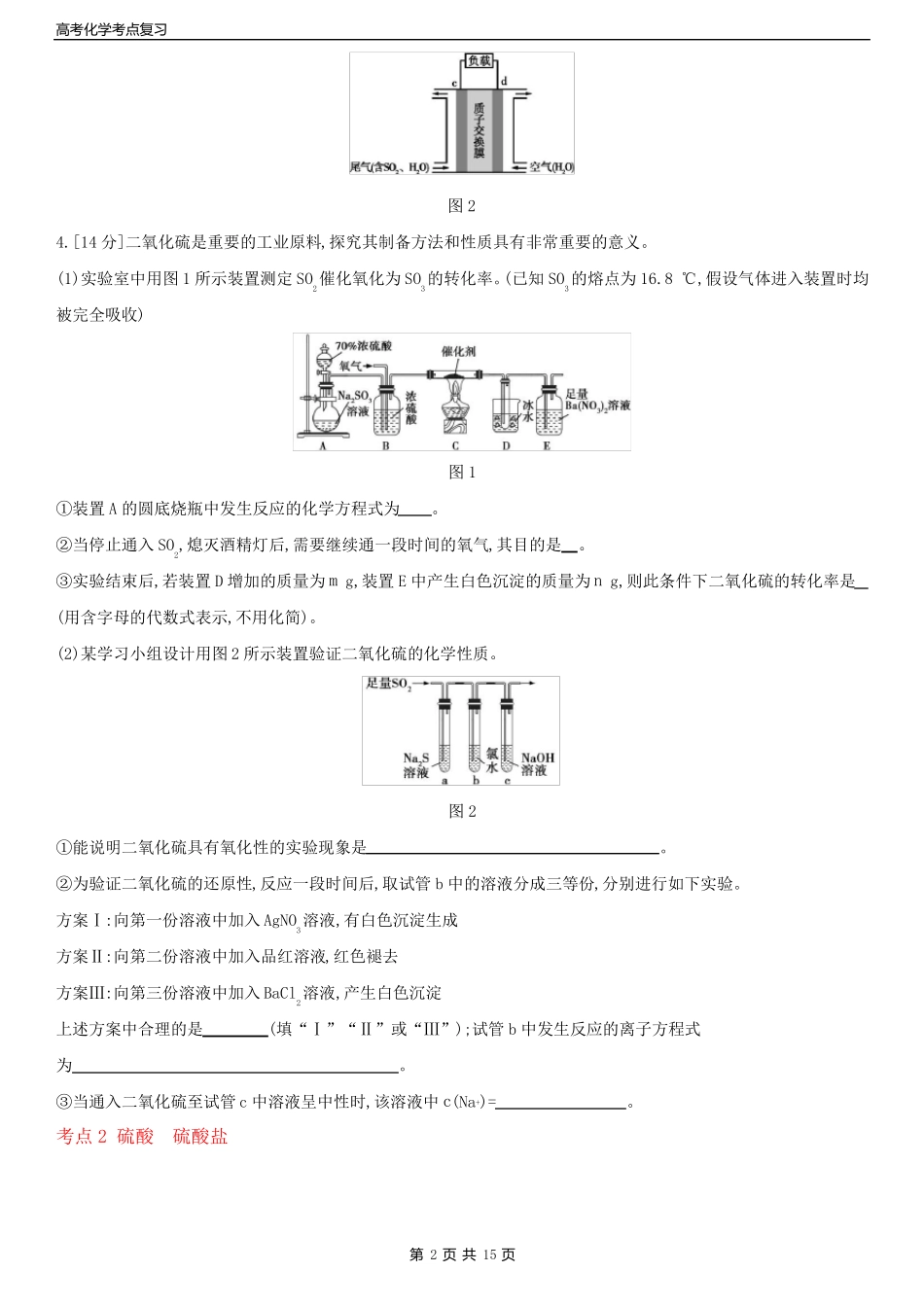
[14分]二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义
(1)实验室中用图1所示装置测定SO2催化氧化为SO3的转化率
(已知SO3的熔点为16
8℃,假设气体进入装置时均被完全吸收)图1①装置A的圆底烧瓶中发生反应的化学方程式为
②当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是
③实验结束后,若装置D增加的质量为mg,装置E中产生白色沉淀的质量为ng,则此