练习册P79无机工业流程题能够以真实的工业生产过程为背景,能够综合考查学生各方面的基础知识及将已有知识灵活应用在生产实际中解决问题的能力
要求同学们既要熟知工业生产的基本原理,又要对流程图中所给出的信息进行提取、筛选,所以这类题成为近年来高考的必考题型
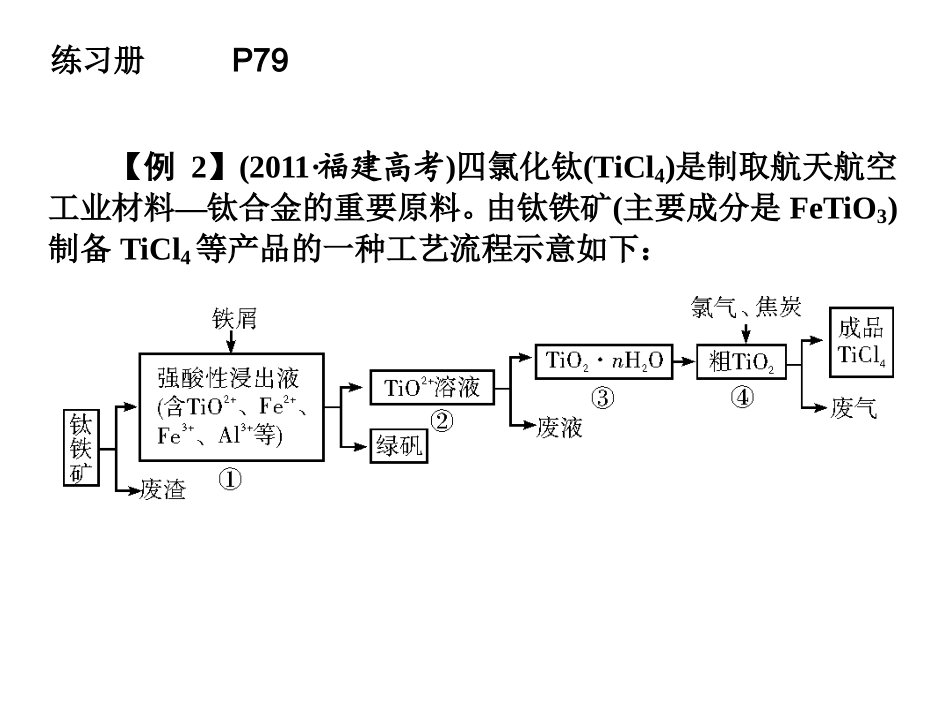
【例2】(2011·福建高考)四氯化钛(TiCl4)是制取航天航空工业材料—钛合金的重要原料
由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:练习册P79回答下列问题:(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性
该过程中有如下反应发生:2Fe3++Fe===3Fe2+2TiO2+(无色)+Fe+4H+===2Ti3+(紫色)+Fe2++2H2OTi3+(紫色)+Fe3++H2O===TiO2+(无色)+Fe2++2H+加入铁屑的作用是______________________________________________
将Fe3+还原成Fe2+,生成Ti3+,保护Fe2+不被氧化(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在________________________________范围
(3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉
已知25℃时,KSP[Fe(OH)3]=2
79×10-39,该温度下反应Fe(OH)3+3H+Fe3++3H2O的平衡常数K=____________
10-9~10-7m(或其他合理答案)2
79×103(4)已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g)ΔH=+140kJ·mol-12C(s)+O2(g)===2CO(g)ΔH=-221kJ·mol-1写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热