第十单元酸和碱课题1常见的酸和碱(第1、2课时)加入紫色石蕊溶液后的颜色变化加入无色酚酞溶液后的颜色变化食醋石灰水盐酸氢氧化钠溶液知识1:红色蓝色红色蓝色无色红色无色红色酸碱指示剂一
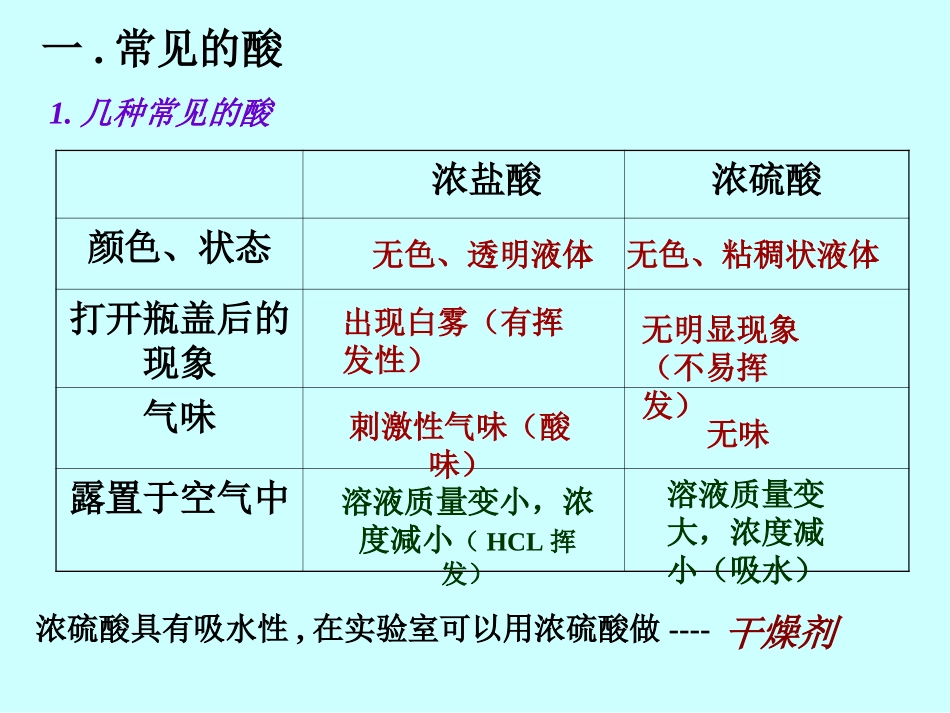
几种常见的酸浓盐酸浓硫酸颜色、状态打开瓶盖后的现象气味露置于空气中无色、透明液体出现白雾(有挥发性)无色、粘稠状液体无味刺激性气味(酸味)无明显现象(不易挥发)干燥剂在实验室可以用浓硫酸做----浓硫酸具有吸水性,溶液质量变小,浓度减小(HCL挥发)溶液质量变大,浓度减小(吸水)2
浓硫酸的强腐蚀性—脱水性(碳化)实验放置一会儿后的现象用玻璃棒蘸浓硫酸在纸上写字用小木棍蘸少量浓硫酸把浓硫酸滴到一小块布上纸张由黄色变成黑色并穿洞变黑布会穿洞,并变成黑色归纳:浓硫酸的性质:(1)吸水性(作干燥剂)(2)强腐蚀性—脱水性(使物质碳化)课前五分钟1
胃酸中含有________,可以帮助消化
下列物质暴露在空气中,质量变大且浓度变小的是()A
NaOH固体B
一杯浓盐酸露天放置,它的浓度和质量有何变化
盐酸答:浓度变小,质量变小
B在稀释浓硫酸时,一定要把________沿器壁慢慢注入____里,并不断_______
切不可将______到进______
注意:浓硫酸水搅拌水酸浓硫酸的稀释:酸入水,沿内壁,缓慢倒,不断搅思考:顺序反了会怎样
-----液滴飞溅,伤人
酸的化学性质加紫色石蕊溶液加无色酚酞溶液稀盐酸稀硫酸红色红色无色无色(1)酸与指示剂的作用(2)酸与金属的反应----放出氢气与稀盐酸反应与稀硫酸的反应镁锌铁Mg+2HCl=H2+ZnCl2Mg+H2SO4=H2+MgSO4Zn+2HCl=H2+ZnCl2Zn+H2SO4=H2+ZnSO4Fe+2HCl=H2+FeCl2Fe+H2SO4=H2+FeSO4(3)酸与金属氧化物反应---生成盐和