(人教2003课标版)【问题引入】第ⅠA族(除H以外)的元素又称为什么元素
包括哪些元素
它们为何排在第ⅠA族
•第ⅠA族元素(除H以外)又称为碱金属元素•因为它们的原子最外层都只有一个电子,所以排在第ⅠA族•这些元素包括:锂、钠、钾、銣、铯、钫(Li)(Na)(K)(Rb)(Cs)(Fr)放射性元素1
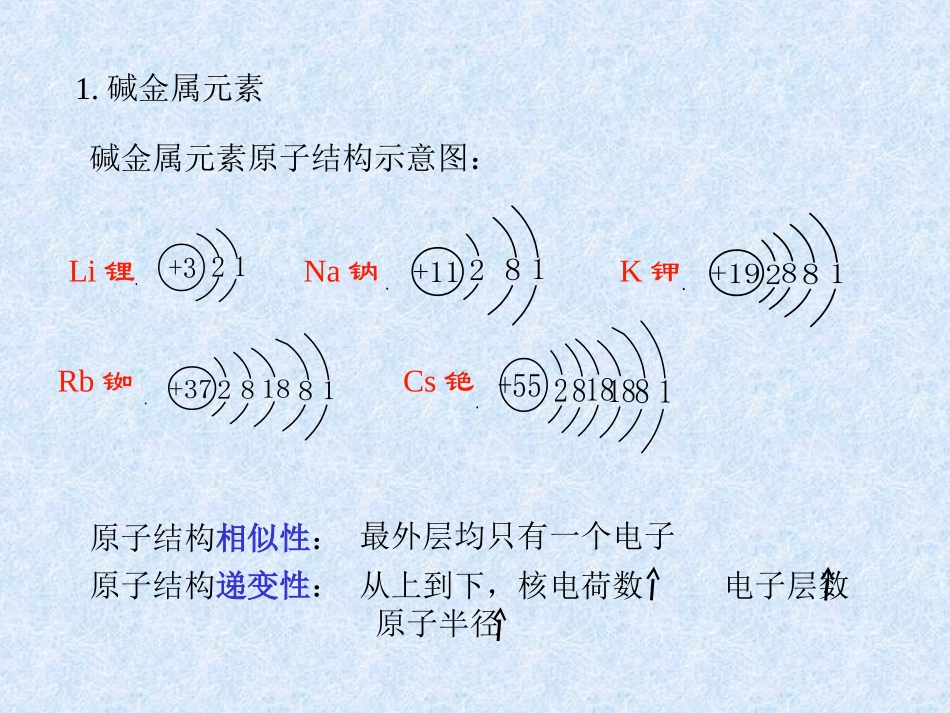
碱金属元素81281818+55812818+378128+19812+11+321Na钠K钾Li锂Rb铷Cs铯碱金属元素原子结构示意图:原子结构相似性:最外层均只有一个电子原子结构递变性:从上到下,核电荷数电子层数原子半径钠与钾性质对比实验:钾在空气中燃烧钾与水反应钠与水反应现象:K更易与水反应,且反应更剧烈Na、K都易与O2反应,但K先燃烧碱金属元素的单质的性质:1、与非金属单质的反应:(氧化锂)4Li+O2===2Li2O点燃2Na+O2===Na2O2点燃(过氧化钠)2、与水反应2Li+2H2O==2LiOH+H22Na+2H2O==2NaOH+H22K+2H2O==2KOH+H2K+O2===KO2点燃(超氧化钾)+1+1+1+1+1+1LiNaKRbCs1
相似性:1)都易失电子表现强还原性2)化合物中均为+1价总结:碱金属的原子结构与性质的关系2
递变性:核电荷数电子层数失电子能力单质还原性元素金属性原子半径化学性质相似最外层上都只有一个电子核对最外层电子的引力金属性:金属原子失电子的能力11、金属与水或者酸反应生成氢气的剧烈程度、金属与水或者酸反应生成氢气的剧烈程度来比较;来比较;22、最高价氧化物对应水化物、最高价氧化物对应水化物————氢氧化物的氢氧化物的碱性强弱来比较
碱性强弱来比较
碱性:KOH>NaOH金属性:K>Na总结:碱金属的主要物理性质LiNaKRbCs1
递变性:1)1
银白色有金属光泽(铯略带金色)2)硬度小,都较柔软,有延