第1讲无机非金属材料的主角考点一•1碳、硅元素在自然界中的存在方式•碳:既有游离态又有化合态•硅:只有化合态
硅在地壳中的含量占第二位
•2性质•金刚石:熔点高,硬度大•石墨:硬度小,电的良导体•硅:具有正四面体结构,为带有金属光泽的灰黑色固体,熔点高,硬度大,质脆•用途:金刚石用作切割刀具,石墨用作电极、铅笔芯;•硅:半导体材料、太阳能电池和合金材料
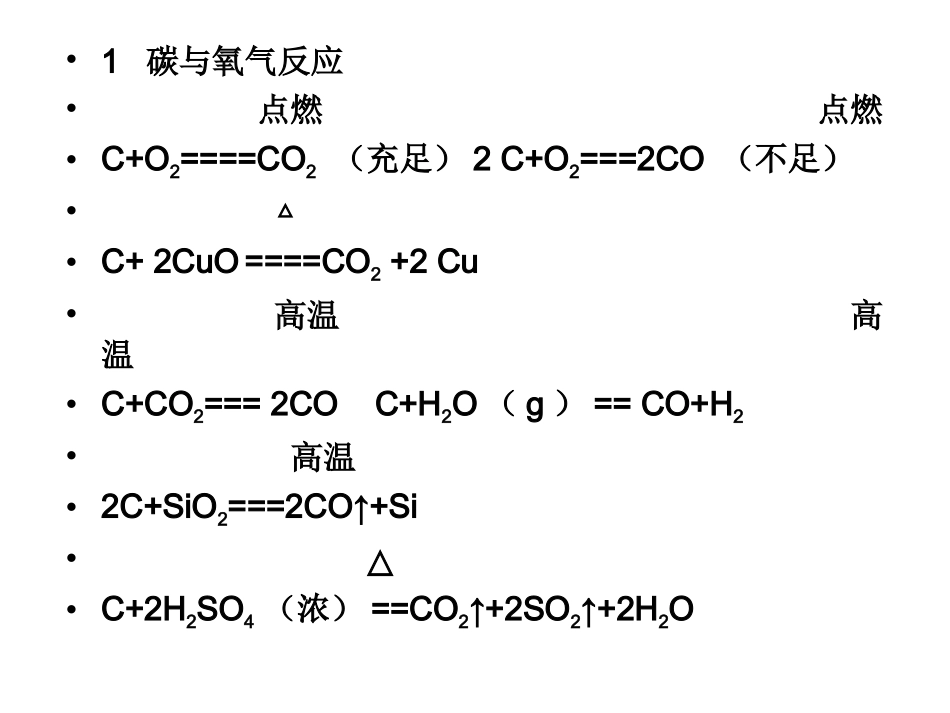
•1碳与氧气反应•点燃点燃•C+O2====CO2(充足)2C+O2===2CO(不足)•△•C+2CuO====CO2+2Cu•高温高温•C+CO2===2COC+H2O(g)==CO+H2•高温•2C+SiO2===2CO↑+Si•△•C+2H2SO4(浓)==CO2↑+2SO2↑+2H2O•2硅的化学性质--还原性•硅不能被浓硫酸、浓硝酸等强氧化剂;常温下,与氟气、氢氟酸、氢氧化钠溶液反应;加热或高温与氧气、氯气反应•△△•Si+O2===SiO2Si+2Cl2===SiCl4•Si+2F2===SiF4•Si+4HF===SiF4↑+2H2↑•Si+2NaOH+H2O==Na2SiO3+2H2↑硅的工业制法•工业上,用焦炭在电炉中还原二氧化碳得到含有少量杂质的粗硅高温•2C+SiO2===2CO↑+Si•粗硅提纯•(1)高温高温•Si+Cl2===SiCl42H2+SiCl4===Si+4HCl•(2)250-300℃•2Si+3HCl=======SiHCl3+H2(SiHCl3三氯甲硅烷)•铜粉或银粉1100-1200℃SiHCl3+H2=======Si+3HCl考点二碳、硅的氧化物•1CO的性质•无色无味的气体,难溶于水,能使人中毒
原因,与人体中血红蛋白相结合,因缺氧而中毒•化学性质:可燃性和还原性•点燃高温2CO+O2==CO23CO+Fe2O3==2Fe+3CO2•2CO2的性质•二氧化碳的熔沸点比二氧