抓住题型、分析考点、总结答题技巧、归纳命题方式迎战高考,应全力以赴内江六中高2016届二轮热点专题复习——无机综合(化工流程+实验+原理)【考纲展示】1
了解科学、技术、社会的相互关系(如化学与生活、材料、能源、环境、生命过程、信息技术的关系等)和在化工生产中遵循“绿色化学”思想的重要性
能结合海水、金属矿物等自然资源综合利用的实例,运用物质性质和反应规律实现物质间的转化
理解氧化还原反应的有关概念及其本质,掌握常见氧化还原反应的配平和计算
了解化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作用
了解吸热反应、放热反应、反应热、焓变等概念
了解热化学方程式的含义,能用盖斯定律进行有关反应焓变的简单计算
理解原电池和电解池的工作原理,了解常见化学电源的种类及其工作原理
了解原电池和电解池的应用
【热点分析】1
化学工艺流程题解决的问题主要有以下几个方面(将原料转化为产品的生产原理问题;除杂、分离和提纯产品等问题;提高产量和效率问题;节能减排,“绿色化学”,循环利用等生产问题;生产设备、流程和生产成本等工艺问题
核心知识点(预处理的各种方法;中心过程涉及的的主要反应;盐溶液的分离提纯方法;平衡原理的应用;原电池和电解工业中的电极反应方程式书写;循环利用的物质的判断;条件的控制及试剂的选择如:温度,PH值;盖斯定律的应用等)3
实验基本操作知识的考察(沉淀的洗涤;沉淀洗净的检验;溶液到晶体的基本操作;晶体失去结晶水的条件及操作;典型离子检验的实验设计)4
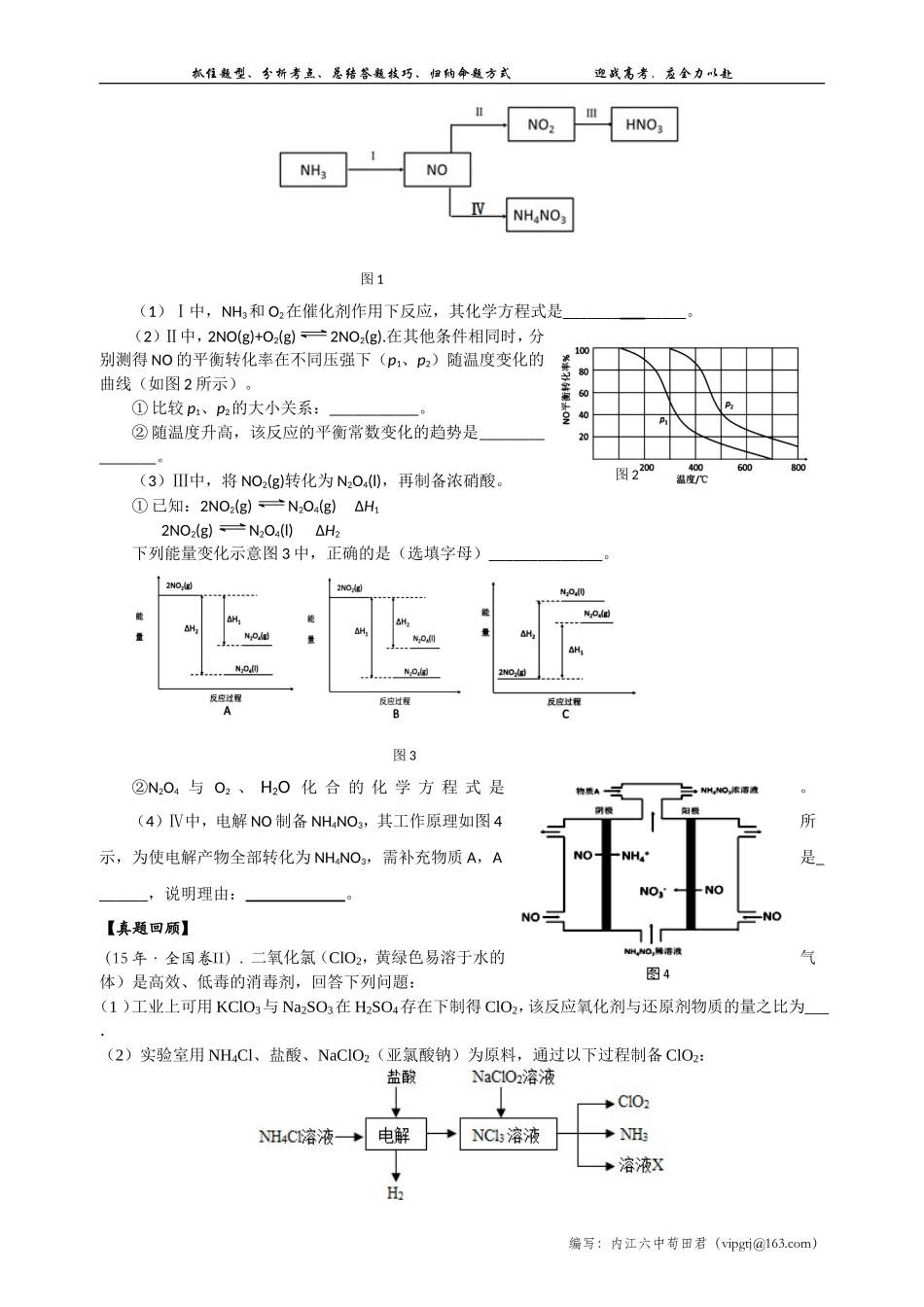
教材基础工艺(铝土矿的提纯;硝酸工业;海水资源的开发利用;纯碱工业等)【流程模型】【题型示例】NH3经一系列反应可以得到HNO3和NH4NO3,如图1所示
编写:内江六中苟田君(vipgtj@163
com)图2抓住题型、分析考点、总结答题技巧、归纳命题方式迎战高考,应全力以赴图1(1)