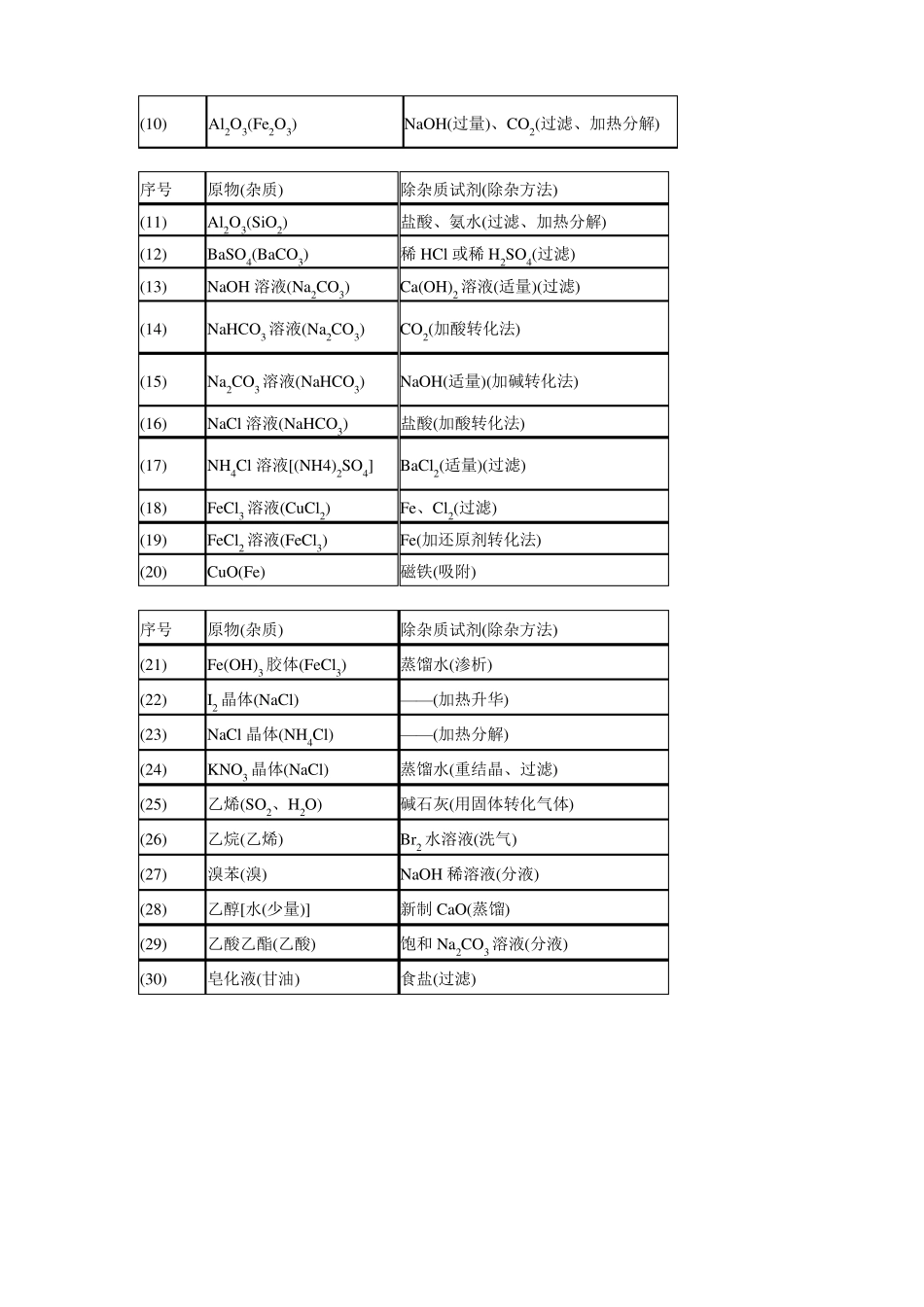
最全高中化学物质的检验、鉴定、除杂1.离子检验的常用方法有三种:检验方沉淀法法焰色反应显色法气体法含义常用碱金属元反应中有沉淀产生反应中有颜色素如:Na、K反应中有气体或溶解变化等离子检验产生2.常见的分离和提纯的方法比较方法适用范围装置从液体中分净化食用过滤离不溶的固水体③定量试验防止过滤药物损失从食盐的分离溶于溶水溶液中蒸发剂中的固体提取食盐溶质晶体加热,用余热蒸干适用方法范围利用互溶液银球的位置应在蒸馏烧瓶体中各成分蒸馏沸点的不同进行分离的2/3,也不能少于1/3④冷凝管中冷却水下进上出水盛放液体不能超过其容积制取蒸馏支管口处③蒸馏烧瓶中所①蒸馏烧瓶中放少量碎瓷片,防止暴沸②温度计水装置应用实例注意事项大量晶体析出时停止过程要不断搅拌,有易被氧气氧化②蒸发①溶质不易分解、不滤器中)洗涤沉淀物应用实例注意事项①要注意一贴二低三靠②必要时要(在过方法适用范围装置应用实例注意事项利用溶质在互不相溶的溶剂里溶解性的不同,用一种溶剂萃取把溶质从它与另一种溶剂所组成的溶液中提取出来的方法把两种互不相溶,密度也不相分液同的液体分离开的方法①萃取剂和溶剂互不相溶、不反应;溶质在萃用有机溶剂(如四氯取剂中溶解度较大,且化碳)从碘水中萃取不反应;萃取剂和原溶碘剂密度相差较大②酒精易溶于水,一般不能做萃取剂①下层液体从下口流出,上层液体从上口倒把CCl4和NaOH溶出②要及时关闭活塞,液分开防止上层液体从下口流出特别提醒混合物的分离与提纯,重在理解物质的性质,并根据性质考虑所采取的方法。一般应注意:①先考虑是否能用物理方法分离与提纯,再考虑用化学方法分离与提纯。②认真分析被提纯物质的性质,选择的试剂应只和杂质反应,而不与主要物质反应。③不能改变被提纯物质的性质,若在除杂过程中,主要物质转化为其他物质,则应使其再次转化为原物质。④含多种杂质的分离与提纯,还要注意所加入试剂的顺序与用量,并遵守不得引入新杂质的原则。3.常见混合物的分离和提纯方法总结序号(1)(2)(3)(4)(5)(6)(7)(8)(9)原物(杂质)N2(O2)CO(CO2)CO2(CO)CO2(HCl)SO2(HCl)Cl2(HCl)CO2(SO2)炭粉(MnO2)炭粉(CuO)除杂质试剂(除杂方法)灼热的铜丝网(用固体转化气体)NaOH溶液(洗气)灼热的CuO(用固体转化气体)饱和NaHCO3溶液(洗气)饱和NaHSO3溶液(洗气)饱和食盐水(洗气)饱和NaHCO3溶液(洗气)浓盐酸(需加热)(过滤)稀盐酸(过滤)(10)序号(11)(12)(13)(14)(15)(16)(17)(18)(19)(20)序号(21)(22)(23)(24)(25)(26)(27)(28)(29)(30)Al2O3(Fe2O3)NaOH(过量)、CO2(过滤、加热分解)原物(杂质)Al2O3(SiO2)BaSO4(BaCO3)NaOH溶液(Na2CO3)NaHCO3溶液(Na2CO3)Na2CO3溶液(NaHCO3)NaCl溶液(NaHCO3)NH4Cl溶液[(NH4)2SO4]FeCl3溶液(CuCl2)FeCl2溶液(FeCl3)CuO(Fe)原物(杂质)Fe(OH)3胶体(FeCl3)I2晶体(NaCl)NaCl晶体(NH4Cl)KNO3晶体(NaCl)乙烯(SO2、H2O)乙烷(乙烯)溴苯(溴)乙醇[水(少量)]乙酸乙酯(乙酸)皂化液(甘油)除杂质试剂(除杂方法)盐酸、氨水(过滤、加热分解)稀HCl或稀H2SO4(过滤)Ca(OH)2溶液(适量)(过滤)CO2(加酸转化法)NaOH(适量)(加碱转化法)盐酸(加酸转化法)BaCl2(适量)(过滤)Fe、Cl2(过滤)Fe(加还原剂转化法)磁铁(吸附)除杂质试剂(除杂方法)蒸馏水(渗析)——(加热升华)——(加热分解)蒸馏水(重结晶、过滤)碱石灰(用固体转化气体)Br2水溶液(洗气)NaOH稀溶液(分液)新制CaO(蒸馏)饱和Na2CO3溶液(分液)食盐(过滤)4.常见离子的检验方法(1)常见阳离子的检验阳离子检验方法反应的离子方程式H+能使紫色石蕊试液或橙色的甲基橙试液++Zn+2H===Zn2+H2↑变为红色。能与锌或碳酸钠(或碳酸钙)反-+CO32+2H===CO2↑+H2O应产生无色气体铵盐(或浓溶液)与NaOH溶液共热,放出+-使湿润的红色石蕊试纸变蓝的有刺激性NH4+OH===NH3↑+H2O气味的NH3+NH4+Na、K+用焰色反应来检验时,它们的火焰分别呈黄色、浅紫色(通过蓝色钴玻璃片观察)能与NaOH溶液反应生成白色沉淀,该沉+-Mg2+2OH===Mg(OH)2↓淀不溶于NaOH溶液能与稀硫酸或可溶性硫酸盐溶液反应产2+-Ba+SO42===BaSO4↓生白色沉淀,且沉淀不溶于稀盐酸Mg2+Ba2+阳离子检验方法反应的...