图1化学平衡图像专题训练解题思路:一看轴(纵、横坐标的意义),二看线(线的走向和变化趋势),三看点(起点、折点、交点、终点、零点的意义),四看要不要作辅助线(等温线、等压线、平衡线),五看量的变化(如浓度变化、温度变化等),六想规律(外界条件对反应速率的影响规律和化学平衡移动规律),七作判断,做出答案
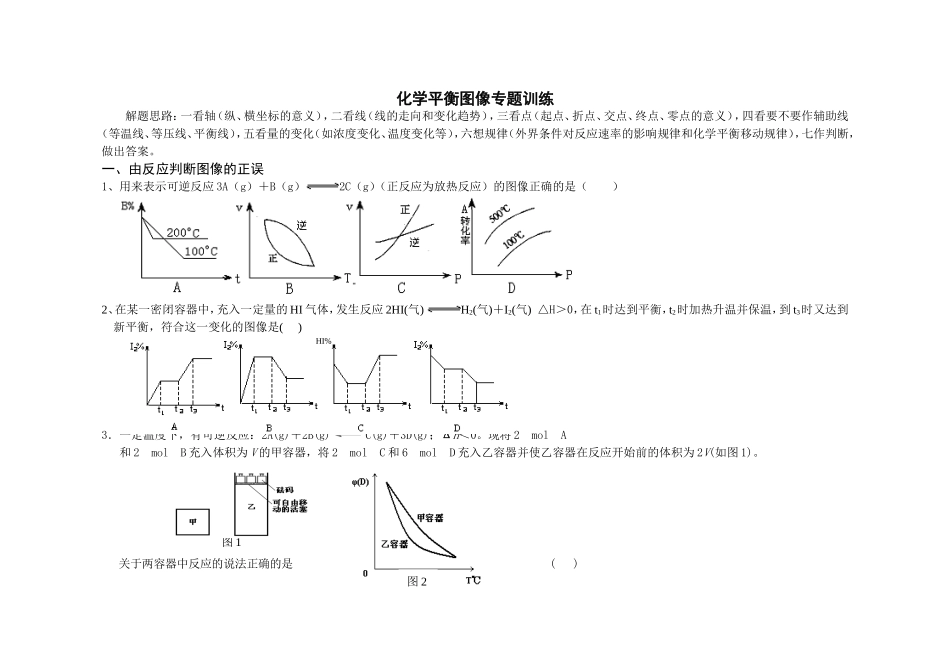
一、由反应判断图像的正误1、用来表示可逆反应3A(g)+B(g)2C(g)(正反应为放热反应)的图像正确的是()2、在某一密闭容器中,充入一定量的HI气体,发生反应2HI(气)H2(气)+I2(气)△H>0,在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是()3.一定温度下,有可逆反应:2A(g)+2B(g)C(g)+3D(g);ΔH<0
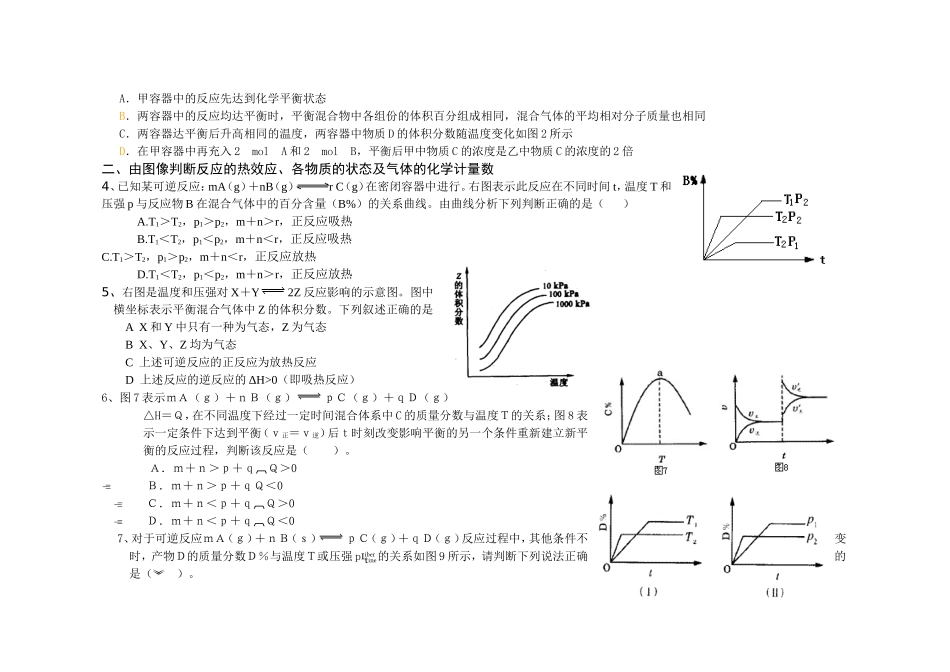
现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图1)
关于两容器中反应的说法正确的是()HI%图2A.甲容器中的反应先达到化学平衡状态B.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量也相同C.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示D.在甲容器中再充入2molA和2molB,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍二、由图像判断反应的热效应、各物质的状态及气体的化学计量数4、已知某可逆反应:mA(g)+nB(g)rC(g)在密闭容器中进行
右图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线
由曲线分析下列判断正确的是()A
T1>T2,p1>p2,m+n>r,正反应吸热B
T1<T2,p1<p2,m+n<r,正反应吸热C
T1>T2,p1>p2,m+n<r,正反应放热D
T1<T2,p1<p2,m+n>r,正