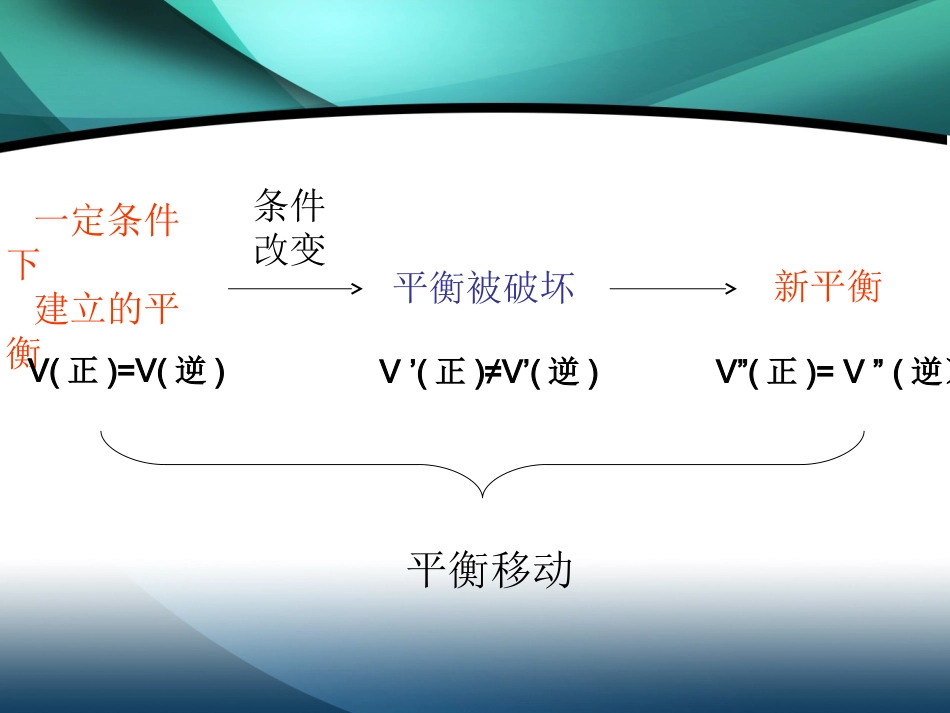
化学平衡的移动“逆”“等”“动”“定”“变”化学平衡的特点:——可逆反应——V正=V逆≠0——动态平衡——平衡时各组分的含量保持恒定——外界条件改变,平衡变化条件改变平衡移动一定条件下建立的平衡平衡被破坏新平衡V(正)=V(逆)V’(正)≠V’(逆)V”(正)=V”(逆)浓度温度压强催化剂【回忆】影响化学反应速率的外界条件主要有哪些
化学反应速率一、化学平衡的移动定义:改变外界条件,引起正、逆反应速率变化,破坏原有的平衡状态,建立起新的平衡状态的过程
研究对象:移动的本质原因:移动的标志:移动方向:已建立的化学平衡状态外界条件改变导致v正≠v逆混合物中各组分的含量发生改变v正>v逆v正<v逆v正=v逆平衡向正方向移动平衡向逆正方向移动平衡不移动二、化学平衡移动的影响因素1、浓度的变化对化学平衡的影响实验1ACr2O72-+H2O2CrO42-+2H+橙色黄色已知在K2Cr2O7的溶液中存在着如下平衡演示:(实验1)向试管中加入4ml0
1mol/LK2Cr2O7溶液;再滴加数滴1mol/LNaOH溶液,观察溶液颜色变化
(实验2)将上述溶液分成两分,向其中一份中滴加11mol/LHNO3溶液,观察溶液颜色变化,并和另一份溶液作对比
思考一:A组:1、试管中加入NaOH的目的是什么
改变了什么条件
2、试管中加入HNO3的目的是什么
改变了什么条件
说明:当其他条件不变时:增大反应物浓度,瞬间v正,v逆,v正v逆,随后v正逐渐,v逆逐渐,最终v正v逆,平衡向移动
增大不变减小增大>=正反应方向结论:结论:其它条件不变的情况下其它条件不变的情况下①①增大反应物浓度或减小生成物浓度平衡向正方向移动增大反应物浓度或减小生成物浓度平衡向正方向移动②②增大生成物浓度或减小反应物浓度平衡向逆方向移动增大生成物浓度或减小反应物浓度平衡向逆方向移动1、浓度的变化对化学平衡的影响结论t1v”正