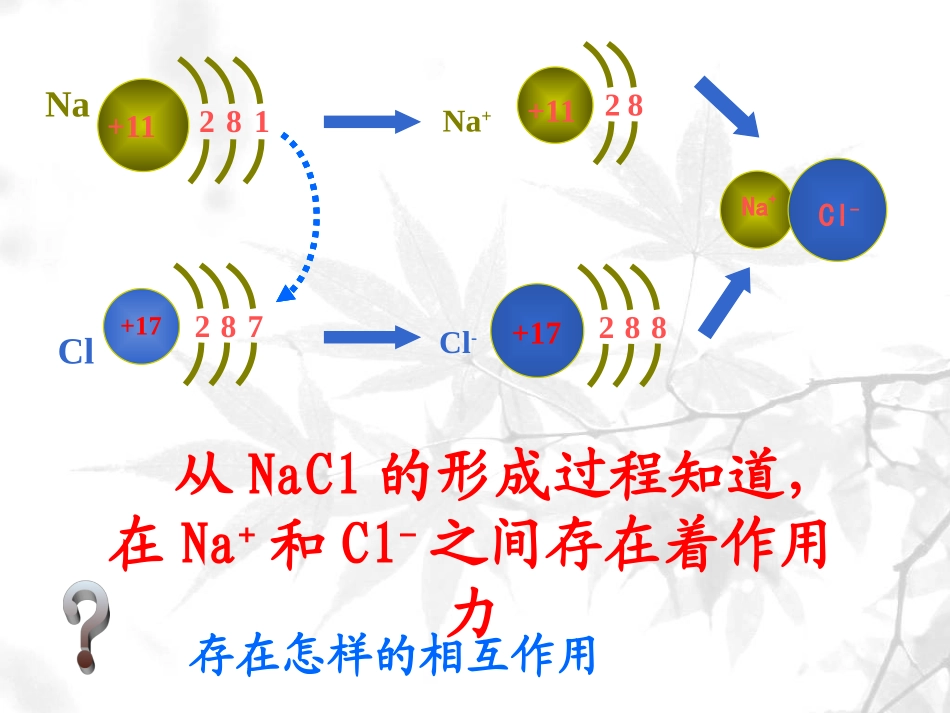
第一章物质结构元素周期律第三节化学键关键词:“相邻的”“强烈的”相邻的两个或多个原子之间强烈的相互作用叫做化学键化学键的类型离子键共价键金属键化学键Na+11812Cl+17872Na+Cl-+1182+17882Na+Cl-从NaCl的形成过程知道,在Na+和Cl-之间存在着作用力存在怎样的相互作用Na和Cl发生反应,Na失去了一个电子,Cl就得到这个电子,双方都达到了8电子的稳定结构,形成了带正电荷的Na+和带负电荷的Cl-,Na+和Cl-之间有静电相互吸引作用;同时电子和电子之间、原子核和原子核之间有相互排斥作用
当两种离子接近到某一距离时,吸引作用和排斥作用达到平衡,于是,阴、阳离子之间就形成了稳定的化合物
一、离子键离子键:阴、阳离子间通过静电作用形成的化学键③核外电子与核外电子间的排斥作用
(1)静电作用①带正电的离子与带负电的离子间的吸引作用;②原子核与原子核间的排斥作用;⑵成键的主要原因:⑶成键微粒:⑷键的本质:⑸成键元素:电子得失阴阳离子静电作用活泼的金属元素与活泼的非金属元素(6)哪些物质能形成离子键
活泼的金属元素(IA,IIA)和活泼的非金属元素(VIA,VIIA)之间的化合物
活泼的金属元素和酸根离子形成的盐3
铵根离子和酸根离子(或活泼非金属元素)形成的盐
式中:“+”表示“相遇”;“”表示“形成”
用电子式表示离子化合物的形成过程:ClNaClNaSKKkS2-k①阳离子须标明电荷数,阴离子要用方括号括起来,并标明电荷数如:Al、②相同的原子、离子要单个写
③不能把“”写成“”
用电子式表示粒子及离子化合物的形成过程时,注意3+S2-小结阴离子阳离子离子化合物活泼金属原子活泼非金属原子失去电子得到电子静电作用静电吸引=静电排斥离子键离子键:使阴、阳离子结合成化合物的静电作用
[讨论]氢气与氯气是如何形成氯化氢的
原子与原子是如何结合形成