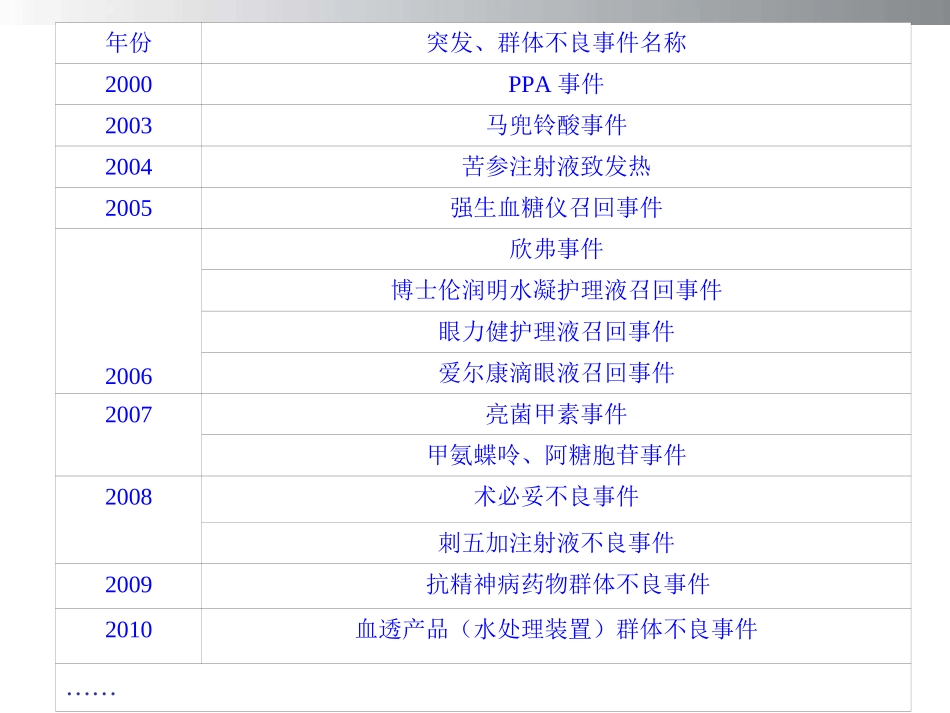
药械突发、群体不良事件调查处置工作方法年份突发、群体不良事件名称2000PPA事件2003马兜铃酸事件2004苦参注射液致发热2005强生血糖仪召回事件2006欣弗事件博士伦润明水凝护理液召回事件眼力健护理液召回事件爱尔康滴眼液召回事件2007亮菌甲素事件甲氨蝶呤、阿糖胞苷事件2008术必妥不良事件刺五加注射液不良事件2009抗精神病药物群体不良事件2010血透产品(水处理装置)群体不良事件……主要内容工作职责与程序定义、分级及适用范围目的法规依据主要内容工作职责与程序定义、分级及适用范围目的法规依据1
法规依据1《药品不良反应报告和监测管理办法》(卫生部令第81号)4《医疗器械不良事件监测与再评价管理办法》(国食药监械[2008]766号)5《医疗器械不良事件监测工作指南》(国食药监械[2011]425号)3《药品和医疗器械安全突发事件应急预案(试行)》(国食药监办[2011]370号)2《药品和医疗器械突发性群体不良事件应急预案》(国食药监办[2005]329号)•《药品不良反应报告和监测管理办法》(27-32条)(卫生部令第81号)••••••••第27条药品生产、经营企业和医疗机构获知或者发现药品群体不良事件后,应当立即通过电话或者传真等方式报所在地的县级药品监督管理部门、卫生行政部门和药品不良反应监测机构,必要时可以越级报告;同时填写《药品群体不良事件基本信息表》,对每一病例还应当及时填写《药品不良反应/事件报告表》,通过国家药品不良反应监测信息网络报告
第28条设区的市级、县级药品监督管理部门获知药品群体不良事件后,应当立即与同级卫生行政部门联合组织开展现场调查,并及时将调查结果逐级报至省级药品监督管理部门和卫生行政部门
第29条药品生产企业获知药品群体不良事件后应当立即开展调查,详细了解药品群体不良事件的发生、药品使用、患者诊治以及药品生产、储存、流通、既往类