专题二:分子、原子、离子博乐市第八中学:杨胜文心中有数:1
分子、原子、离子的概念
原子、离子的结构或分类
分子和原子,原子和离子的异同比较
运用用分子、原子的观点解释一些现象
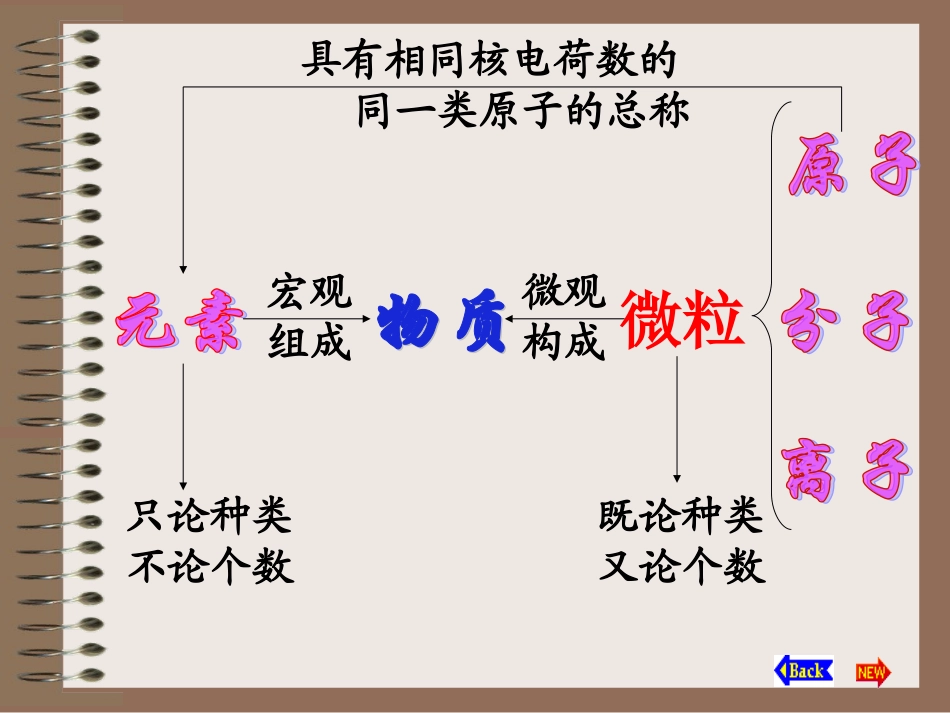
微观构成宏观组成只论种类不论个数既论种类又论个数具有相同核电荷数的同一类原子的总称微粒分子原子离子分裂构成得失电子微粒的性质1
体积小、质量小;肉眼看不见
微粒在不断地运动中
微粒之间存在着空隙
直接构成O2、N2、H2直接构成金属如:Fe、Cu等直接构成酸、碱、盐构成物质的微粒表示方法:化学式表示方法:元素符号表示方法:离子符号H2O、CO2等物质稀有气体单质C、S、P、Si等失得电子概念:原子核核外电子质子中子原子离子的分类阴离子(-):核内质子数核外电子数保持物质化学性质的最小粒子化学变化中的最小粒子原子的结构:核电荷数=质子数=核外电子数带电的原子或原子团离子:核电荷数=质子数≠核外电子数带负电荷带正电荷不带电(+)(不带电)+17第1层第2层第3层原子核质子数287结构示意图电子层该电子层上的电子数思考:你读出了什么
氯原子的结构示意图原子核带正电氯离子的结构示意图17+288NaNaMgMg221188+11+11222288+12+12226688+16+16227788+17+17SSClCl2288+11+112288+12+12228888+16+16228888+17+171
要能够分清原子结构示意图、离子结构示意图要能够分清原子结构示意图、离子结构示意图2
要能够根据示意图写出对应的符号要能够根据示意图写出对应的符号原子原子:核电荷数=核外电子数:核电荷数=核外电子数离子:核电荷数≠核外电子数离子:核电荷数≠核外电子数NaNa++MgMg22++SS22--ClCl--阴离子(-):核内质子数核外电子数根据右边的结构图回答:根据右边的结构图回答:•