专题十无机工艺流程分析(7)1、下列制备物质的工业生产流程合理的是()A
制镁:海水Mg(OH)2MgOMgB
由NaCl制漂白剂:NaCl(aq)Cl2漂白粉C
由铝土矿冶炼铝:铝土矿AlD
合成NH3:NH4Cl和Ca(OH)2固体NH3纯净干燥的氨气2、磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一,采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是()A
合理处理废旧电池有利于保护环境和资源再利用B
从"正极片"中可回收的金属元素有Al、Fe、LiC
"沉淀"反应的金属离子为Fe3+D
上述流程中可用硫酸钠代替碳酸钠3、根据如图海水综合利用的工业流程图,判断下列说法正确的是()已知:MgCl2•6H2O受热生成Mg(OH)Cl和HCl气体等
过程①加入的药品顺序为:Na2CO3溶液→BaCl2溶液→NaOH溶液→过滤后加盐酸B
过程②通过氧化还原反应可产生1种单质版权所有©正确教育侵权必纠
在过程③中将MgCl2•6H2O直接灼烧得到MgCl2D
在过程④、⑥反应中每氧化0
2molBr-需消耗标准状况下2
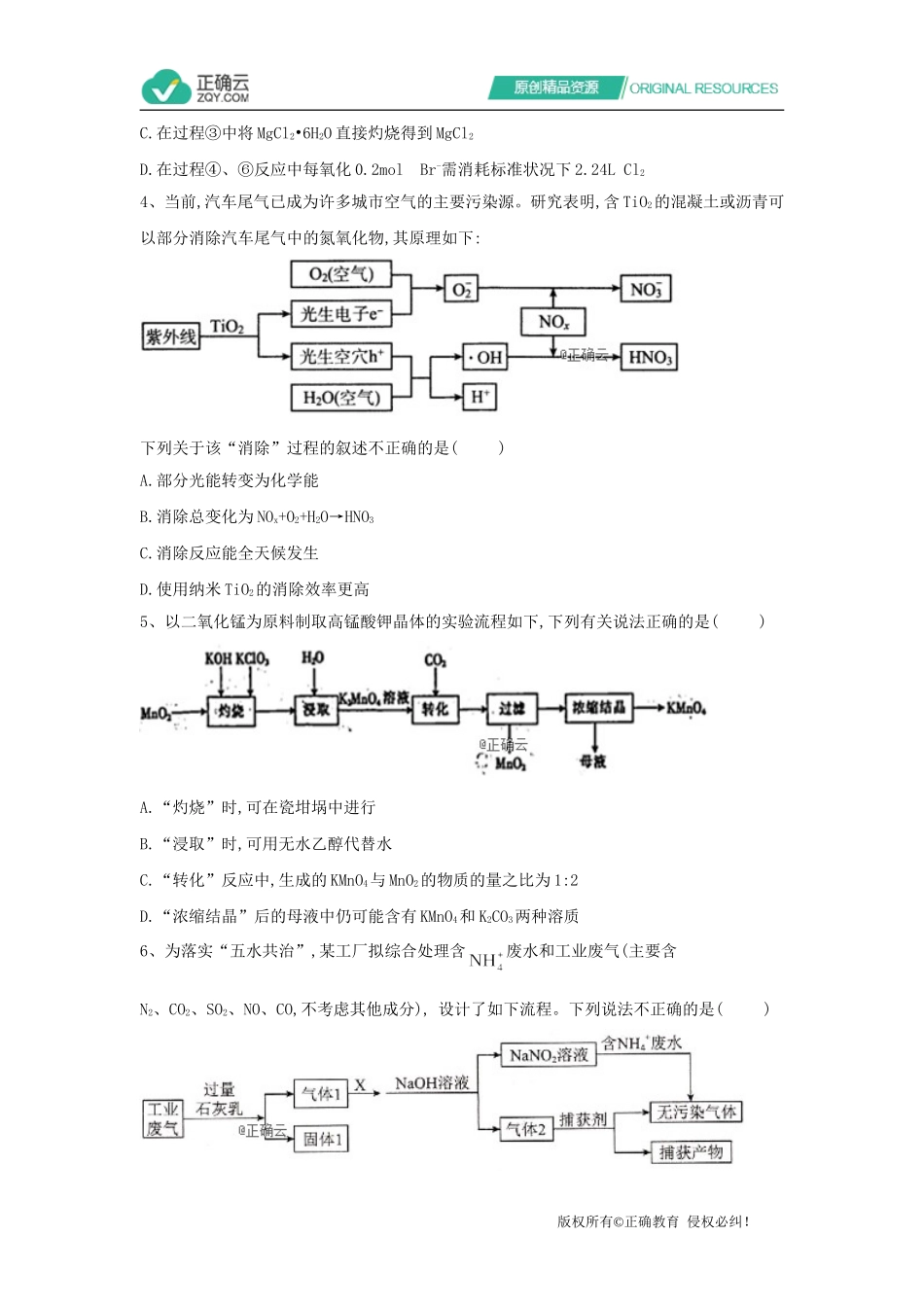
24LCl24、当前,汽车尾气已成为许多城市空气的主要污染源
研究表明,含TiO2的混凝土或沥青可以部分消除汽车尾气中的氮氧化物,其原理如下:下列关于该“消除”过程的叙述不正确的是()A
部分光能转变为化学能B
消除总变化为NOx+O2+H2O→HNO3C
消除反应能全天候发生D
使用纳米TiO2的消除效率更高5、以二氧化锰为原料制取高锰酸钾晶体的实验流程如下,下列有关说法正确的是()A
“灼烧”时,可在瓷坩埚中进行B
“浸取”时,可用无水乙醇代替水C
“转化”反应中,生成的KMnO4与MnO2的物质的量之比为1:2D
“浓缩结晶”后的母液中仍可能含有KMnO4和K2CO3两种溶质6、为落实“五水共治”,某工厂