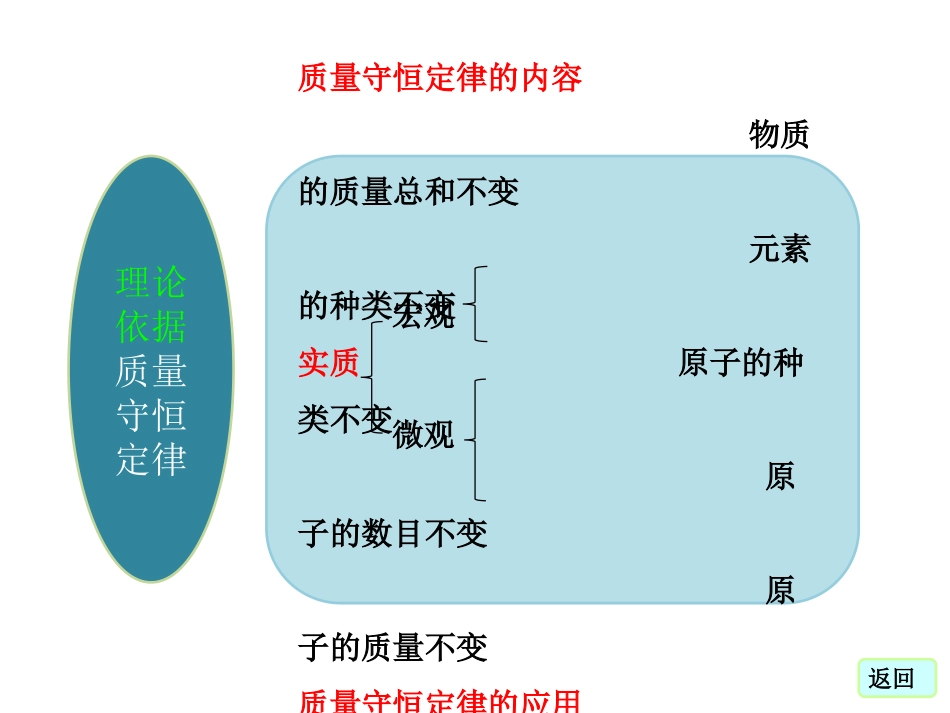
第五单元化学方程式复习课件化学方程式化学方程式理论依据:质量守恒定律应用:根据化学方程式的计算质量守恒定律的内容物质的质量总和不变元素的种类不变实质原子的种类不变原子的数目不变原子的质量不变质量守恒定律的应用理论依据质量守恒定律返回宏观微观化学方程式概念:用化学式表示化学反应的式子表示反应物、生成物和反应条件表示各物质之间的质量比表示参加反应的各粒子的相随数量关系表示反应前后质量守恒化学方程式的读法书写原则:以客观事实为基础,遵守质量守恒定律书写步骤:写、配、注返回含义应用根据化学方程式的计算计算步骤与书写格式根据化学方程式计算的常见类型返回1.一切化学反应都必须遵守______________________,该定律的内容是_________________________________________________________________
2.物质发生化学反应时,只是反应物的原子____________生成新物质,反应前后_______________________________都没有发生改变,因此化学反应前后各物质的___________________一定相等
3.化学方程式是用_____________表示化学反应的式子,书写化学方程式必须遵守的两个原则是___________________________________________
书写化学方程式的步骤依次是:(1)写____________________________________________;(2)配:__________;(3)标:____________________
质量守恒定律参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和重新组合原子的种类、数目、质量质量总和化学式以客观事实为依据;以质量守恒定律为根据左边写反应物的化学式、右边写生成物的化学式配平