化学期末复习三(金属、碳)授课时间2014
21一、金属性质知识整理:有常见的物质A、B、C、D,它们有下图之间的相互关系,回答以下问题:一.若A为铜,A的颜色是
(1)过程①的现象是,反应方程式为(2)过程②能否发生,理由是(3)过程③中金属D可能是,反应的方程式为
二.若A为铁,块状或片状的铁为色,粉末状的铁为色
(1)若B为黑色,则B的化学式为,反应方程式是若B为红棕色,则B的主要成分是,过程①需要的条件为(2)C溶液的颜色是,过程②反应方程式为(3)若D为红色,写出反应的方程式该反应杯称为炼铜
三.若A为镁(1)过程①在生产、生活中的应用是,反应方程式为(2)过程②的现象为,反应方程式为二、炼铁知识整理:1
炼铁的原理是12
图甲为工业炼铁的设备,名称为,进口1所进的原料是,进口2所进的原料是
图中生铁出口比炉渣出口低,原因是
生铁和钢都是和的合金
常见的合金还有、
图乙为实验室研究炼铁的化学原理的装置,请回答和该实验有关的问题
⑴A处玻璃管中发生反应的化学方程式为⑵B处的实验现象_____⑶C处酒精灯的作用______⑷现有含杂质的氧化铁样品10克(杂质不参加反应),为测定该样品中氧化铁的质量分数,某同学用右图所示的装置进行实验,得到如下两组数据:反应前氧化铁完全反应后甲组洗气瓶和石灰水的质量为190g洗气瓶和石灰水的质量为196g乙组玻璃管和氧化铁样品的质量为57.9g玻璃管和氧化铁样品的质量为55.2g你认为应选择___组的数据来计算样品中氧化铁的质量分数,其结果为___
不选另一组的理由是
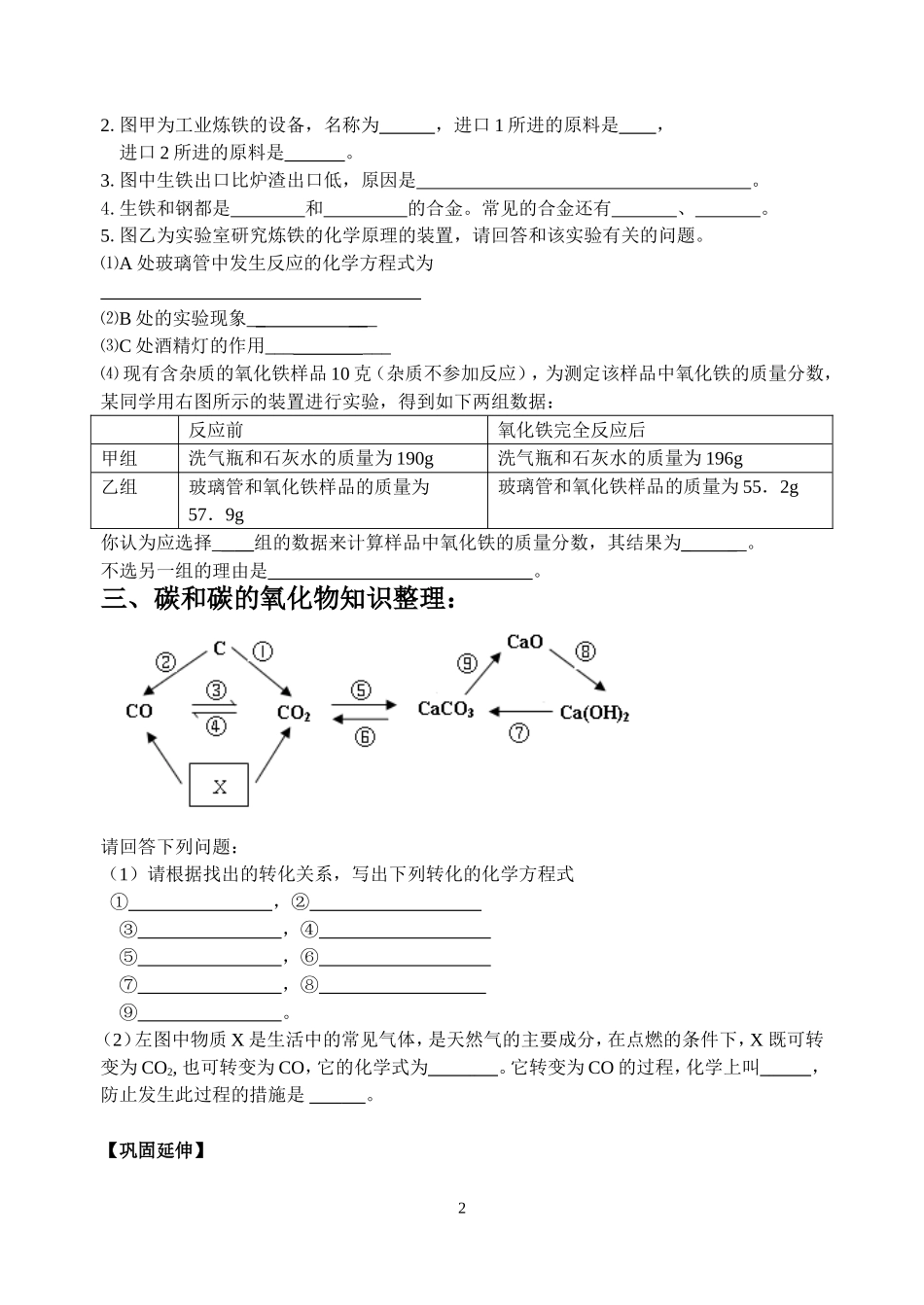
三、碳和碳的氧化物知识整理:请回答下列问题:(1)请根据找出的转化关系,写出下列转化的化学方程式①,②③,④⑤,⑥⑦,⑧⑨
(2)左图中物质X是生活中的常见气体,是天然气的主要成分,在点燃的条件下,X既可转变为CO2,也可转变为CO,它的化学式为