第五章化学反应与能量考试要求教学建议1
认识化学能可以与热能、电能等其他形式能量之间相互转化,能量的转化遵循能量守恒定律
认识化学能与热能的相互转化,恒温恒压条件下化学反应的反应热可以用焓变表示
了解盖斯定律及其简单应用
认识化学能与电能相互转化的实际意义及其重要应用
了解原电池及常见化学电源的工作原理
了解电解池的工作原理,认识电解在实现物质转化和储存能量中的具体应用
了解金属发生电化学腐蚀的本质,知道金属腐蚀的危害,了解防止金属腐蚀的措施
一轮复习不能按部就班地循教材复习,否则会磨灭学生的积极性和创造力
本章将化学能与热能、化学能与电能整合在一起复习,有利于考生从根本上掌握“能量守恒”这一观点,贯通知识联系,形成知识体系
本章共设7课时,仍遵循由基础到能力,由单一到综合的编写路径
更难能可贵的是,由于本章知识与前沿科技热点结合比较紧密,高考更注重对创新问题的考查,故本章在编写时注重前沿热点问题的渗透和应用
第1课时化学能与热能(1)——基本概念一课过(过基础)知识点一焓变、热化学方程式1.化学反应的实质与特征2.焓变、反应热(1)焓(H)用于描述物质所具有能量的物理量
(2)焓变(ΔH)ΔH=H(生成物)-H(反应物),单位kJ·mol-1
(3)反应热当化学反应在一定温度下进行时,反应所放出或吸收的热量,通常用符号Q表示,单位kJ·mol-1
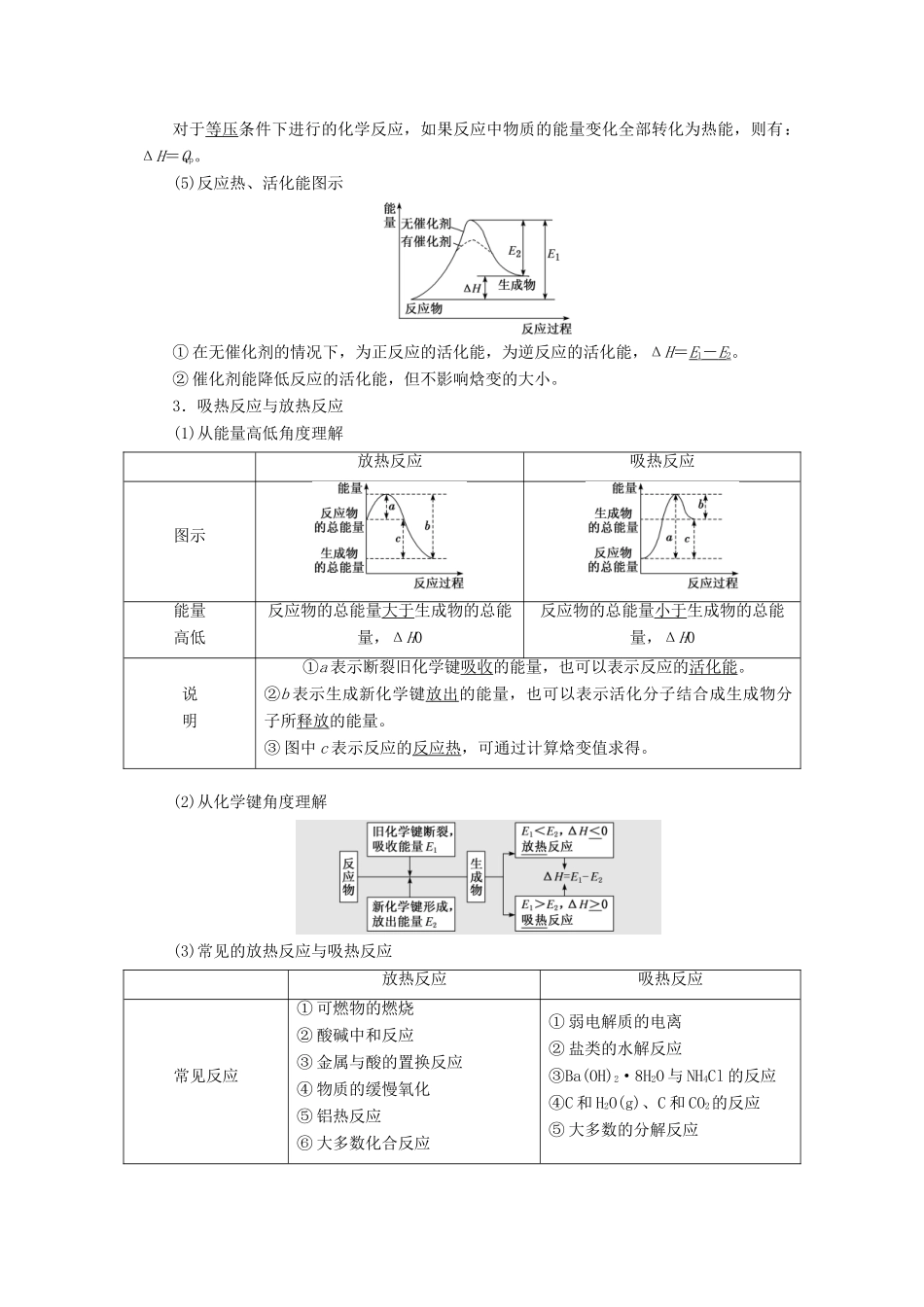
(4)焓变与反应热的关系对于等压条件下进行的化学反应,如果反应中物质的能量变化全部转化为热能,则有:ΔH=Qp
(5)反应热、活化能图示①在无催化剂的情况下,为正反应的活化能,为逆反应的活化能,ΔH=E1-E2
②催化剂能降低反应的活化能,但不影响焓变的大小
3.吸热反应与放热反应(1)从能量高低角度理解放热反应吸热反应图示能量高低反应物的总能量大于生成物的总能量,ΔH0反应物的总能量小于生成物的总能量,