第三章有机化合物第一节最简单的有机化合物——甲烷第1课时甲烷的结构和性质基础梳理一、有机化合物和烃概念组成元素有机化合物大部分含有的化合物一定含有,常含有,有的还含有等
烃仅含有的有机物(写元素符号)碳元素碳元素氢元素、氧元素N、S、P、Cl碳元素和氢元素C、H思维拓展1.含碳元素的化合物都是有机化合物吗
答案不是,有机化合物都含有碳元素,但含有碳元素的物质不一定都是有机物,如CO、CO2、碳酸盐、碳酸氢盐都属于无机物
二、甲烷1.存在和用途(1)存在:甲烷是、、油田气和煤矿坑道气的主要成分
(2)用途:天然气是一种、、的清洁能源,还是一种重要的
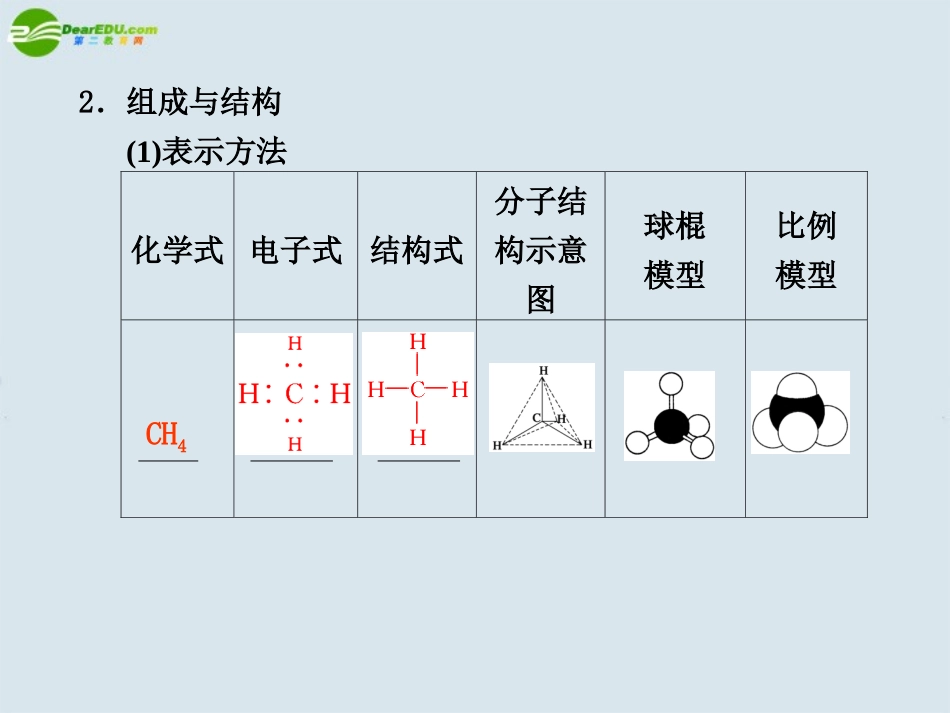
天然气沼气高效低耗污染小化工原料2.组成与结构(1)表示方法化学式电子式结构式分子结构示意图球棍模型比例模型CH4(2)结构特点甲烷分子是以为中心,为顶点的结构,其中C—H键的和相同
碳原子氢原子正四面体键长键角思维拓展2.如何证明甲烷分子是正四面体结构
答案甲烷的正四面体结构,可以通过研究CH2Cl2存在几种结构来确定
CH4有四个等同的C—H键,在空间上可能有两种对称分布:正四面体结构和平面正方形结构,如图所示
若是正四面体结构,甲烷分子中任意两个氢原子被两个氯原子取代,CH2Cl2的结构只有一种;若是平面正方形结构,则取代的两个氢原子分邻位和对位,CH2Cl2的结构有两种
科学研究发现,CH2Cl2的结构只有一种,说明甲烷是正四面体结构
3.物理性质颜色状态气味密度(与空气相比)水溶性4
化学性质通常状况下,甲烷比较稳定,与等强氧化剂不反应,与、也不反应
但在特定的条件下,甲烷也能发生某些反应
无色气态无味小不溶KMnO4强酸强碱(1)氧化反应纯净的甲烷在空气中安静的燃烧,火焰呈,放出大量的热,反应的化学方程式为
(2)取代反应①取代反应:有机化合物分子里的被其他所代替的反应
淡蓝色原子或原子团原子或原子团CH4+