酸碱盐的复习----提纯、鉴别和检验【知识点分析】一、净化与干燥1、气体净化的几种方法吸收法:用吸收剂将杂质气体吸收除去
如,除去CO中混有的少量CO2,可先用浓NaOH溶液吸收CO2,再用浓硫酸等干燥剂除去水蒸气
转化法:通过化学反应,将杂质气体转化为所要得到的气体
如,除去CO2中的少量CO,可将混合气体通过足量的灼热CuO,CO+CuOCu+CO2
常见气体吸收剂见下表:(请讲H2O、O2H2、CO、CO2、HCl等气体杂质填入下表)吸收剂吸收的气体杂质吸收剂吸收的气体杂质水可溶性气体:HCl、NH3等NaOH固体无水CuSO4碱石灰灼热的铜网NaOH溶液灼热的CuO浓硫酸2、气体的干燥气体的干燥是通过干燥剂来实现的,选择干燥要根据气体的性质,一般原则是:酸性干燥剂不能用来干燥碱性气体,碱性干燥剂不能用来干燥酸性气体,干燥装置由干燥剂状态决定
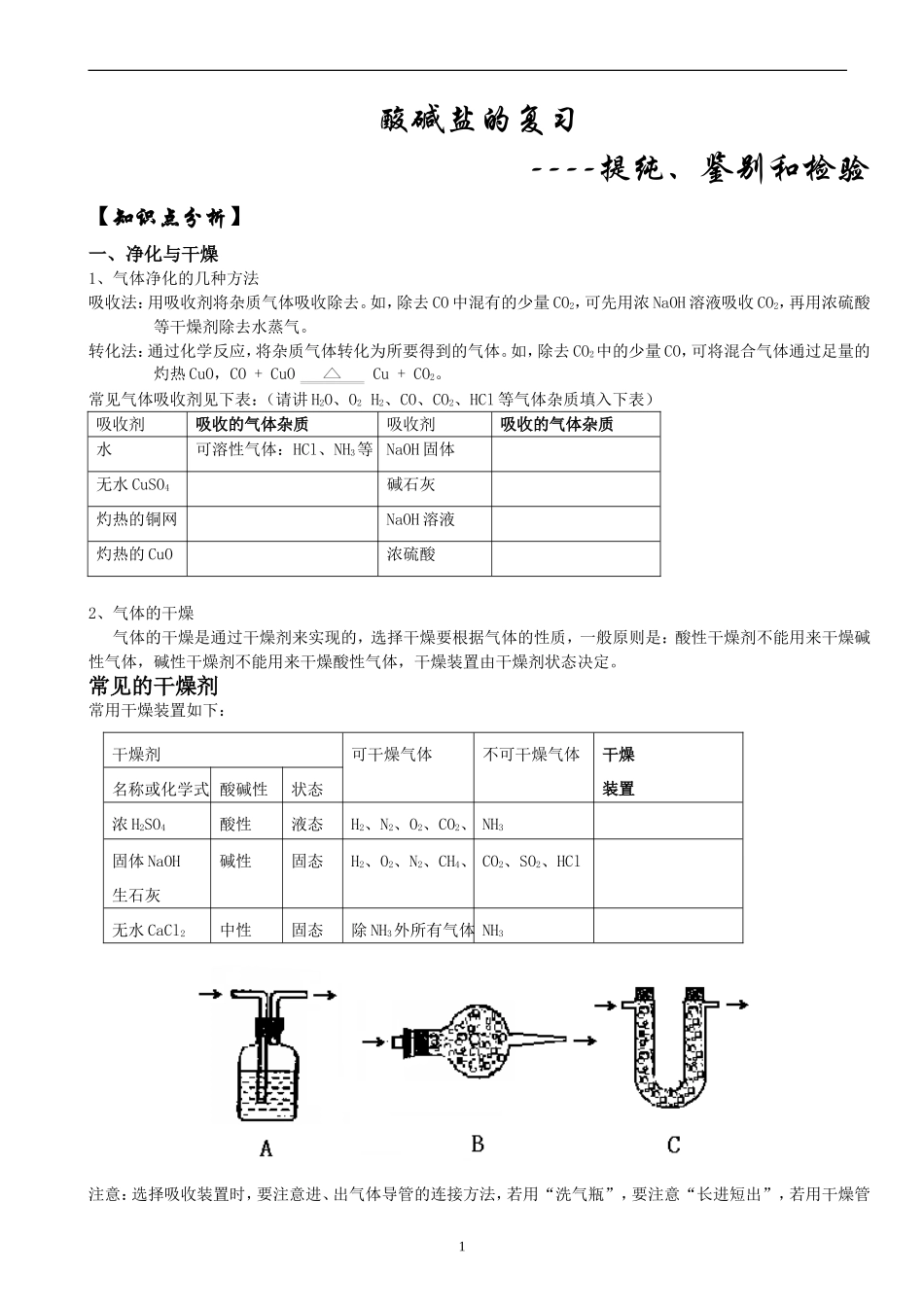
常见的干燥剂常用干燥装置如下:注意:选择吸收装置时,要注意进、出气体导管的连接方法,若用“洗气瓶”,要注意“长进短出”,若用干燥管1干燥剂可干燥气体不可干燥气体干燥装置名称或化学式酸碱性状态浓H2SO4酸性液态H2、N2、O2、CO2、NH3固体NaOH生石灰碱性固态H2、O2、N2、CH4、CO2、SO2、HCl无水CaCl2中性固态除NH3外所有气体NH3要注意“大进小出”
先除去气体中含有的其他杂质,干燥除去水蒸气的操作放在最后
二、物质的分离和提纯分离和提纯的主要方法方法适用范围或原理举例过滤法粗盐的提纯结晶法蒸发从含有HCl的NaCl溶液中分离出固体NaCl降低温度分离NaCl与KNO3的混合物续表方法适用范围或原理举例(写出化学方程式)化学方法化气法与杂质反应生成气体而除去除Na2SO4中Na2CO3,可加适量稀H2SO4:沉淀法将杂质转化为沉淀过滤除去除去NaCl中的Na2SO4,可加适量的BaCl2:置换法将杂质