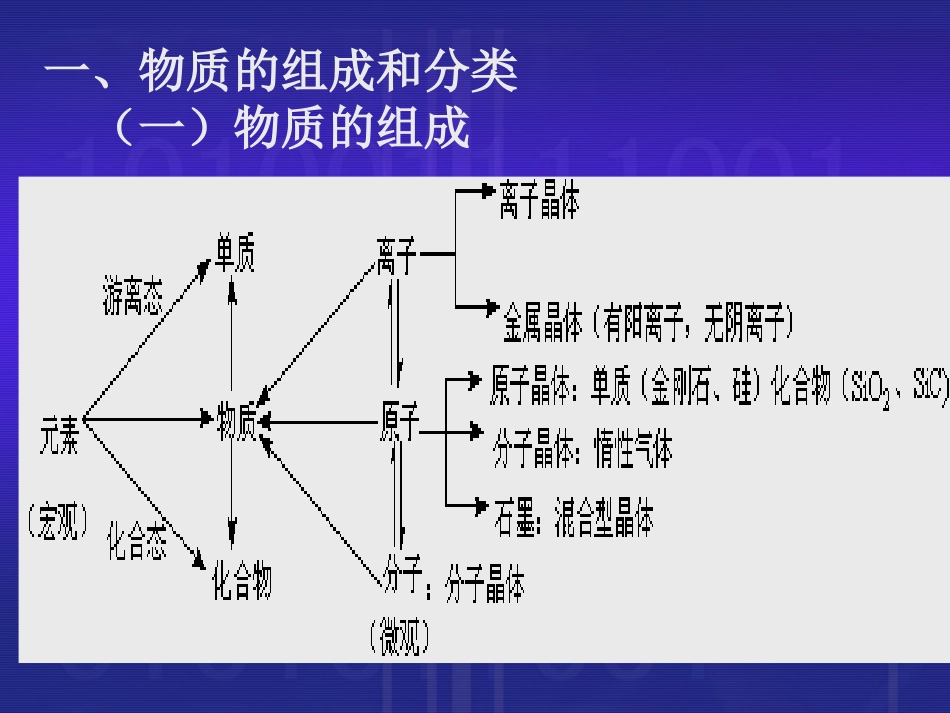
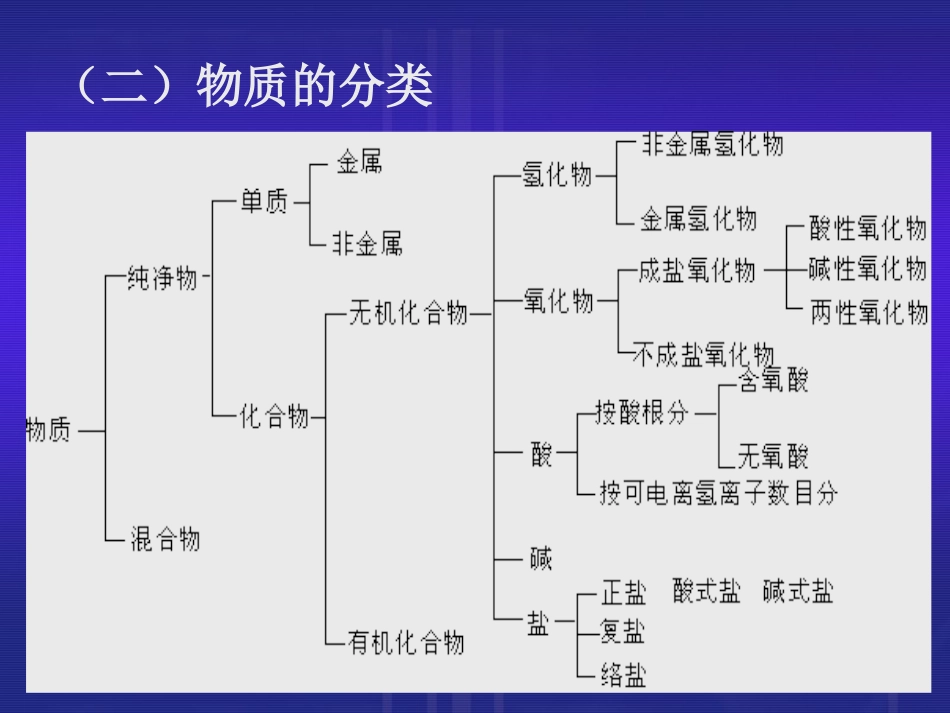
基本概念总复习(一)一、物质的组成和分类(一)物质的组成(二)物质的分类1.判断是否为纯净物的标准:⑴有固定组成:如Fe3O4
由同种分子组成的是纯净物
易错点:由同种元素组成的物质不一定是纯净物,例如:金刚石和石墨混合为混合物;由同种原子组成的物质不一定是纯净物,例如16O2和16O3混合为混合物
⑵有固定熔沸点
如玻璃无固定熔点,为混合物
⑶结晶水合物都是纯净物
例如:明矾(KAl(SO4)2·12H2O)、胆矾(即蓝矾CuSO4·5H2O)、绿矾(FeSO4·7H2O)、皓矾(ZnSO4·7H2O)、芒硝(Na2SO4·10H2O)、生熟石膏(CaSO4·2H2O、2CaSO4·H2O)等
要熟记一些重要物质的化学成分、俗名、用途,明确它们的物质分类
注意:纯净物不是绝对纯的物质
2.混合物:高分子都是混合物;分散系都是混合物
常见无机混合物按主族顺序应记住:ⅠA碱石灰(NaOH+CaO)草木灰(主要成分K2CO3)ⅡA大理石(主要CaCO3),电石(主要CaC2),水垢(CaCO3+Mg(OH)2)ⅢA铝热剂(Al粉和某些金属氧化物)ⅣA玻璃,水泥,陶瓷,黑火药ⅤA王水(体积比(浓HCl:浓HNO3)=3:1)VIIA漂白粉Ⅷ生铁六气:水煤气(CO+H2),天然气(主要成分是甲烷),液化石油气(丙烷、丁烷)有机物:福尔马林,油脂,煤,石油,汽油,凡士林等二、化学用语(一)熟记并正确书写各主族和零族元素的名称、符号和离子符号
(二)能根据化合价正确书写化学式,并能根据化学式判断化合价
(三)明确核外电子排布规律,掌握电子式和原子结构示意图(前20号元素、学过的主族元素和铁)
会用电子式表示物质的形成过程
(四)理解质量守恒定律的含义
能正确书写化学方程式、热化学方程式、离子方程式、电离方程式、电极反应式
明确燃烧热和中和热的定义
三、变化与基本反应类型1.置换反应:⑴