构成物质的微粒(4)学习目标:1
理解为什么要用原子结构示意图表示原子以及表示的方法,清楚原子结构示意图中各部分的意义
了解离子的概念和形成;3
知道原子和离子的异同点学习重点:1
离子的概念和形成;2
原子和离子的异同点【课前尝试】一.原子核外电子的排布1
排布特点能量越低离核越近,能量越高离核越远,分层排布2
排布规律第1层最多排2个;第2层最多排8个;最外层不超过8个二.原子结构示意图【课堂探究】一、试着画出1-20号元素的原子结构示意图:观察得出:原子最外层电子与原子的分类及化学性质间的关系原子分类最外层电子数化学性结论质:稳定性金属原子元素的化学性质由决定
非金属原子稀有气体原子二、离子1
离子也是构成的一种微粒2
离子的形成及分类原子得到电子(电子数质子数),带电荷,称为阴离子;原子失去电子(电子数质子数),带电荷,成为阳离子
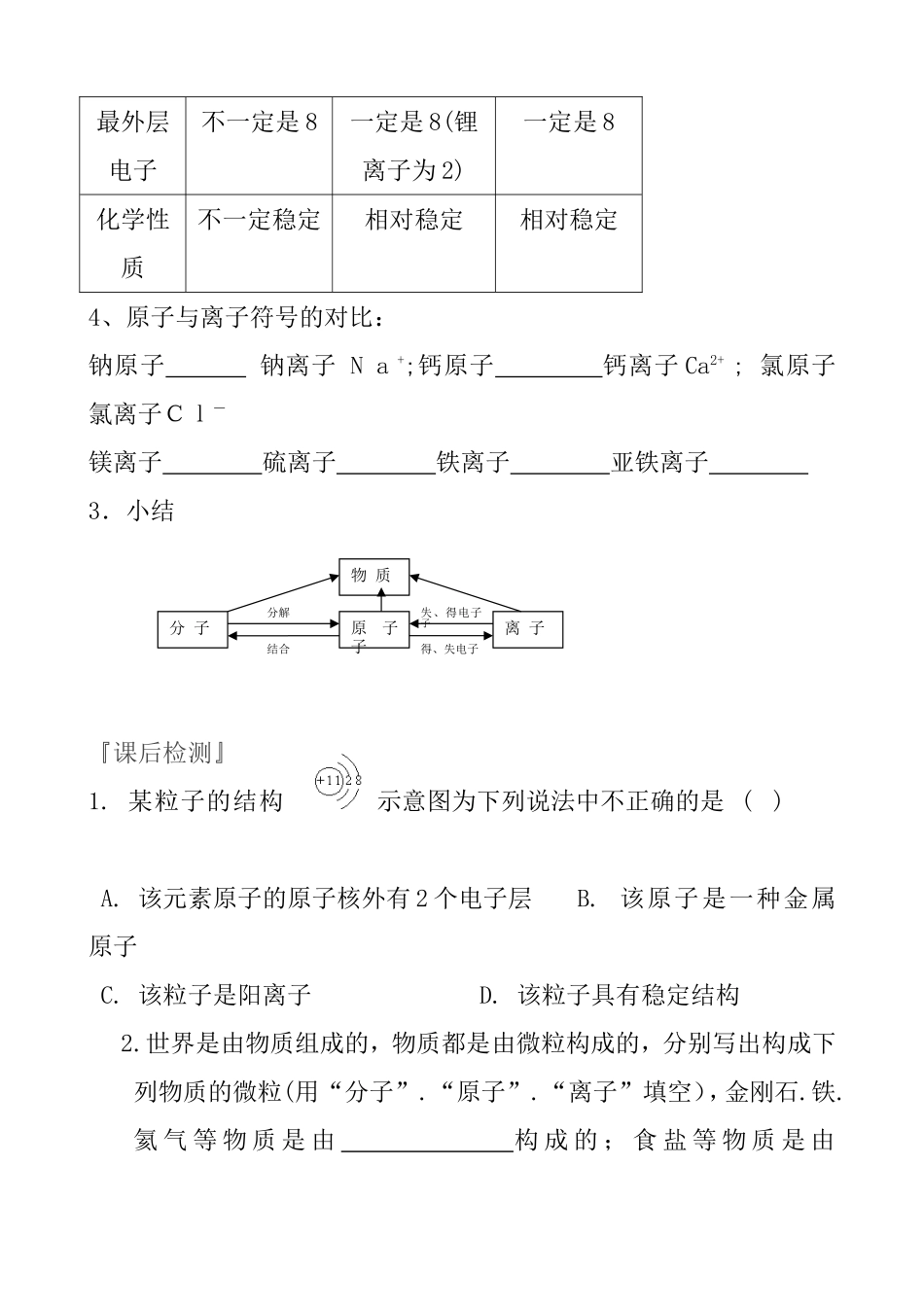
原子与离子的比较微粒原子阳离子阴离子结构质子数=电子数质子数>电子数质子数