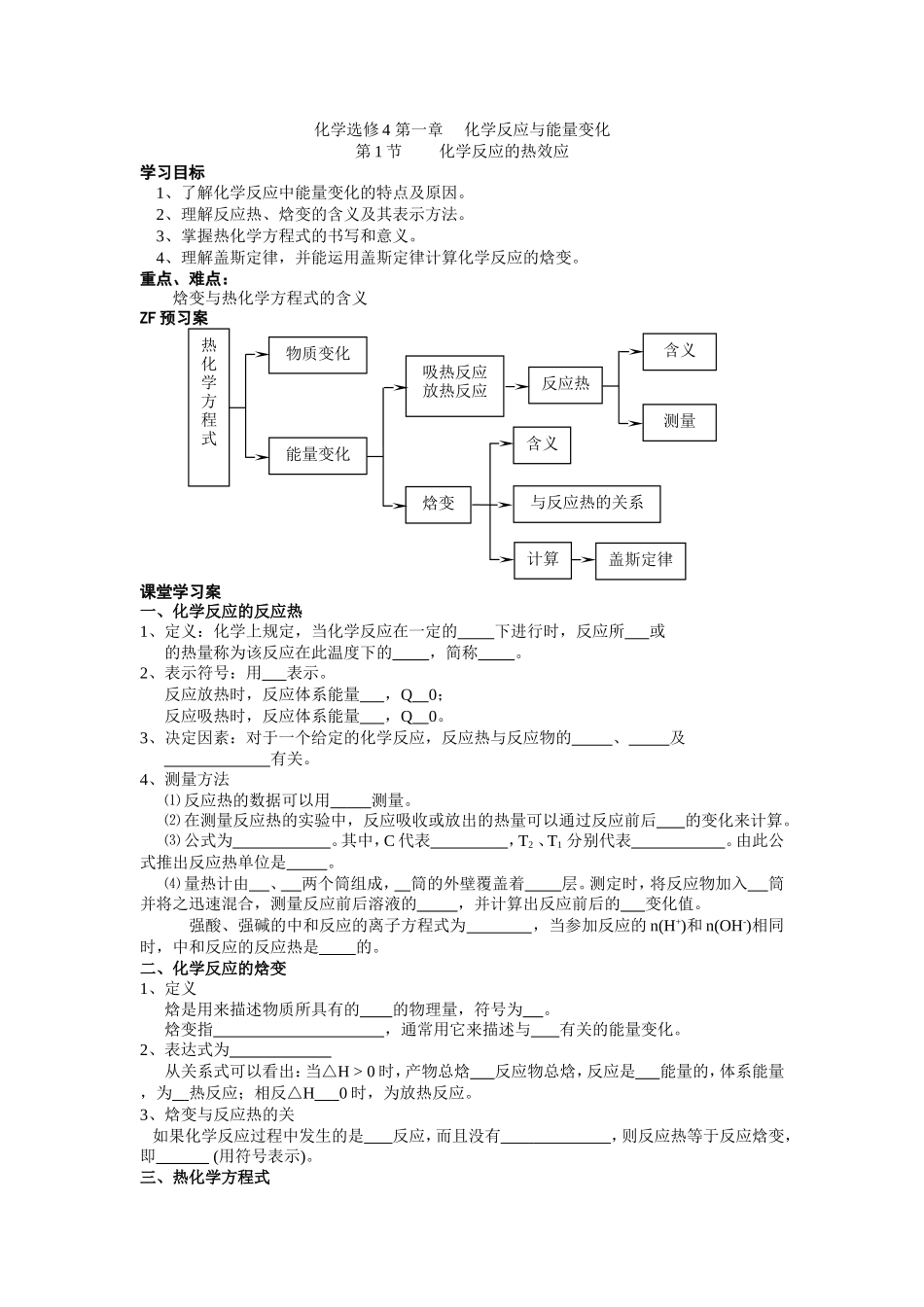
化学选修4第一章化学反应与能量变化第1节化学反应的热效应学习目标1、了解化学反应中能量变化的特点及原因。2、理解反应热、焓变的含义及其表示方法。3、掌握热化学方程式的书写和意义。4、理解盖斯定律,并能运用盖斯定律计算化学反应的焓变。重点、难点:焓变与热化学方程式的含义ZF预习案课堂学习案一、化学反应的反应热1、定义:化学上规定,当化学反应在一定的下进行时,反应所或的热量称为该反应在此温度下的,简称。2、表示符号:用表示。反应放热时,反应体系能量,Q0;反应吸热时,反应体系能量,Q0。3、决定因素:对于一个给定的化学反应,反应热与反应物的、及有关。4、测量方法⑴反应热的数据可以用测量。⑵在测量反应热的实验中,反应吸收或放出的热量可以通过反应前后的变化来计算。⑶公式为。其中,C代表,T2、T1分别代表。由此公式推出反应热单位是。⑷量热计由、两个筒组成,筒的外壁覆盖着层。测定时,将反应物加入筒并将之迅速混合,测量反应前后溶液的,并计算出反应前后的变化值。强酸、强碱的中和反应的离子方程式为,当参加反应的n(H+)和n(OH-)相同时,中和反应的反应热是的。二、化学反应的焓变1、定义焓是用来描述物质所具有的的物理量,符号为。焓变指,通常用它来描述与有关的能量变化。2、表达式为从关系式可以看出:当△H>0时,产物总焓反应物总焓,反应是能量的,体系能量,为热反应;相反△H0时,为放热反应。3、焓变与反应热的关如果化学反应过程中发生的是反应,而且没有,则反应热等于反应焓变,即(用符号表示)。三、热化学方程式热化学方程式物质变化能量变化吸热反应放热反应焓变与反应热的关系计算含义盖斯定律反应热含义测量1、概念将一个化学反应的变化和反应的变化同时表示出来的化学方程式称为热化学方程式。如:2H2(g)+O2(g)=2H2O(l)△H(273K)=-571.6kJ·mol-1表示的含义是2、书写注意事项:①在各物质的后面用括号注明,一般用英文字母、、分别代表物质的气态、液体、固态,水溶液中的溶质则用表示。但不用“↑”“↓”(因已注明状态)。②在△H后要注明,因为在不同的下进行同一个反应,其反应的是不同的。若为298K,可以省略。③标明△H的:吸热表示为“”,放热表示为“”。④△H的单位为。其中,每mol表明参加反应的各物质的物质的量与热化学方程式中各物质的系数相同。⑤热化学方程式的系数指的是反应中各物质的,并不表示物质的分子或原子数,可以是数,也可以是数,若各物质的系数加倍,则△H的也加倍。若反应逆向进行,则△H改变,但不变。【例题1】根据事实,写出298K时下列反应的热化学方程式:(1)1mol氮气与适量氢气起反应,生成2mol氨气,放热92.2KJ热量。(2)1mol碳与适量水蒸气完全反应,生成一氧化碳气体和氢气,吸收131.3KJ热量。【例题2】已知H2(g)+Cl2(g)=2HCl(g)H=-184△.6kJ·mol-1,则反应HCl(g)=1/2H2(g)+1/2Cl2(g)的△H为()A.+184.6kJ·mol-1B.-92.3kJ·mol-1C.-369.2kJ·mol-1D.+92.3kJ·mol-1四、反应焓变的计算对于一个反应,无论是完成还是完成,其反应的是一样的,这一规律称为。即化学反应的反应热只与有关,而与无关。方法:若一个化学方程式可由另外几个化学方程式相加或相减而得到,则该化学反应的焓变即这几个化学方程式焓变的代数和。如由A到B可以设计如下两个途径,则焓变△H、△H1、△H2的关系可以表示为。【例题2】根据下列热化学方程式求Zn(s)+HgO(s)=ZnO(s)+Hg(l)的△H。Zn(s)+1/2O2(g)=ZnO(s)H=-351.1KJ·mol△-1Hg(l)+1/2O2(g)=HgO(s)H=-90.7KJ·mol△-1课堂检测案1、下列各项与反应热的大小无关的是()A.反应物的状态B.温度C.反应物的多少D.表示反应热的单位2、下列说法正确的是()A.若反应是放热反应,则反应物的总能量一定高于生成物的总能量B.焓变是指1mol物质参加反应时的能量变化C.反应放热时△H>0,吸热时△H<0D.如果反应为放热反应,故不必加热就可发生3、已知:298K,101kPa时,合成氨反应的热化学方程式为3H2(g)+N2(g)2NH3(g)△H=-92.38kJ·mol-1。在该温度下,取1molN2(g)和3molH2(g)放在一密闭容器中,在催化剂存在下进行反应,测得反应放出的热量92.38kJ(填>...