学苑新报化学天地学苑新报化学天地电离平衡电离平衡第一节(第二课时)可逆反应有什么特征
化学平衡有什么特可逆反应有什么特征
化学平衡有什么特征
若在纯水滴加冰醋酸,试分析一下所形成若在纯水滴加冰醋酸,试分析一下所形成的水溶液中发生哪些变化
的水溶液中发生哪些变化
以醋酸为例,研究弱电解质的电离过程中以醋酸为例,研究弱电解质的电离过程中实质上包含着哪几个过程
实质上包含着哪几个过程
弱电解质的电离过程中包含:弱电解质的电离过程中包含:((11))分子电离成离子;分子电离成离子;((22))离子结合成分子
离子结合成分子
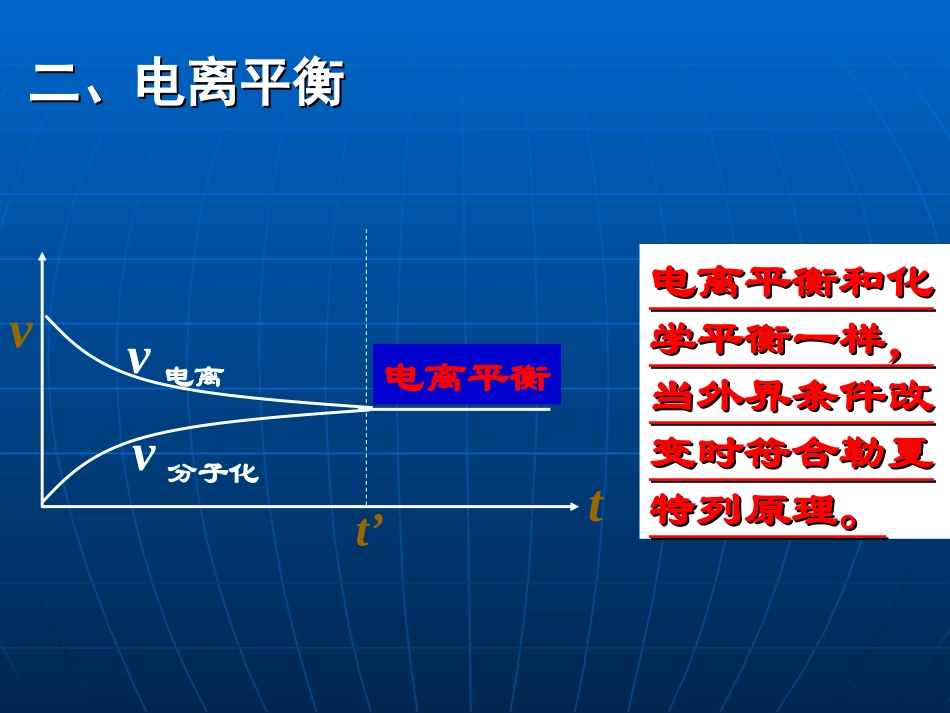
二、电离平衡二、电离平衡vt’tv电离v分子化电离平衡电离平衡和化电离平衡和化学平衡一样,学平衡一样,当外界条件改当外界条件改变时符合勒夏变时符合勒夏特列原理
影响电离平衡有哪些因素影响电离平衡有哪些因素((11)温度)温度电离过程是吸热过程,平衡温度升高向电电离过程是吸热过程,平衡温度升高向电离方向移动
((22)浓度)浓度浓度越大,电离程度越小
浓度越大,电离程度越小
((33)其他因素)其他因素讨论:讨论:11、、在盐酸中加少量在盐酸中加少量NaClNaCl固体,在醋酸溶固体,在醋酸溶液中加少量液中加少量NaAcNaAc固体,将分别对两种酸的电离固体,将分别对两种酸的电离有怎样的影响
有怎样的影响
22、在、在0
1mol/L0
1mol/L醋酸溶液分别:加热、加入醋酸溶液分别:加热、加入少量盐酸、加入少量氢氧化钠、加入醋酸铵晶体,少量盐酸、加入少量氢氧化钠、加入醋酸铵晶体,电离平衡会怎样移动
溶液中电离平衡会怎样移动
溶液中cc(H(H++))怎样变化
33、强电解质溶液中有无可能存在电离平衡
、强电解质溶液中有无可能存在电离平衡
问题:怎样定量的比较弱电解质的相对强弱
电离程度相对大小怎么比较