第三节化学键发展目标体系构建1
以典型物质为例,认识离子键、共价键等化学键的形成,能用电子式对离子键和共价键进行表征,能描述化学键理论模型,并用模型解释和推测物质的组成、结构、性质及变化
培养学生“宏观辨识与微观探析,证据推理与模型认知”的核心素养
能以宏观现象及化学键等不同角度对物质进行分类,能从物质的构成微粒及相互作用说明物质的共性、差异及其原因,解释同类物质的性质变化规律
知道分子存在一定的空间结构
培养学生的“宏观辨识与微观探析”的核心素养
一、离子键和离子化合物1.离子键(1)NaCl的形成示意图钠离子和氯离子通过静电作用结合在一起,形成氯化钠
(2)定义:带相反电荷离子之间的相互作用叫做离子键
(3)成键粒子:阴、阳离子
(4)成键元素:一般是活泼的金属和活泼的非金属
微点拨:离子键的本质是阴、阳离子之间的静电作用,既包括静电吸引也包括静电排斥
2.离子化合物3.电子式(1)概念:在元素符号周围用“·”或“×”来表示原子的最外层电子(价电子)排布的式子
(2)粒子电子式的表示方法粒子电子式的表示方法(举例)原子离子阳离子阴离子化合物(3)用电子式表示离子化合物的形成过程
如NaCl:
微点拨:“·(点)”或“×”都表示电子,二者应用时没有区别
二、共价键和共价化合物1.共价键(1)形成过程(以Cl2的形成为例):(2)定义:原子间通过共用电子对所形成的相互作用
(3)成键粒子:原子
(4)成键元素:一般是同种的或不同种的非金属元素
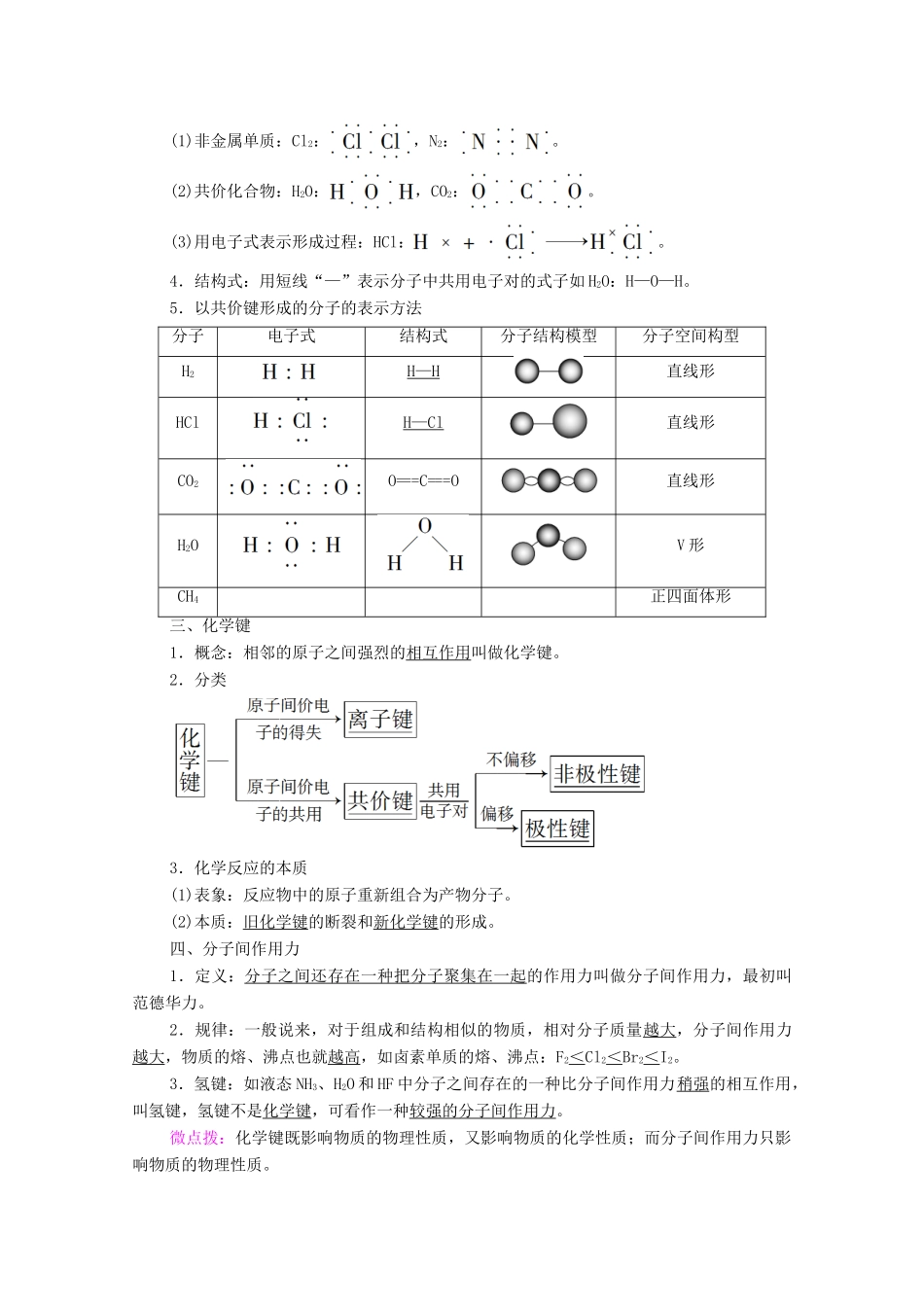
(5)分类2.共价化合物3.电子式(1)非金属单质:Cl2:,N2:
(2)共价化合物:H2O:,CO2:
(3)用电子式表示形成过程:HCl:
4.结构式:用短线“—”表示分子中共用电子对的式子如H2O:H—O—H
5.以共价键形成的分子的表示方法分子电子式结构式分子结构模型分子空间构型H2H—H直线形HClH—Cl直线形CO2