第八章氮族元素第一节氮和磷复习目标展示1.理解氮族元素的相似性、递变性,熟记特殊性
2.了解N2、P(P4)及其氧化物(NO、NO2、N2O4等)、氢化物(NH3)的性质
3.了解氮的氧化物、含磷的洗涤剂等对环境的污染及防治
知识点1氮族元素问题1:怎样根据元素周期律(表)的知识理解氮族元素的相似性和特殊性
氮族元素位于元素周期表的VA族2
氮族元素的特殊性(1)N2是大气的重要组成部分(占78%)
(2)N2不如白磷(P4)性质活泼
(3)Sb和Bi是金属元素;+5价的Bi具有强的氧化性
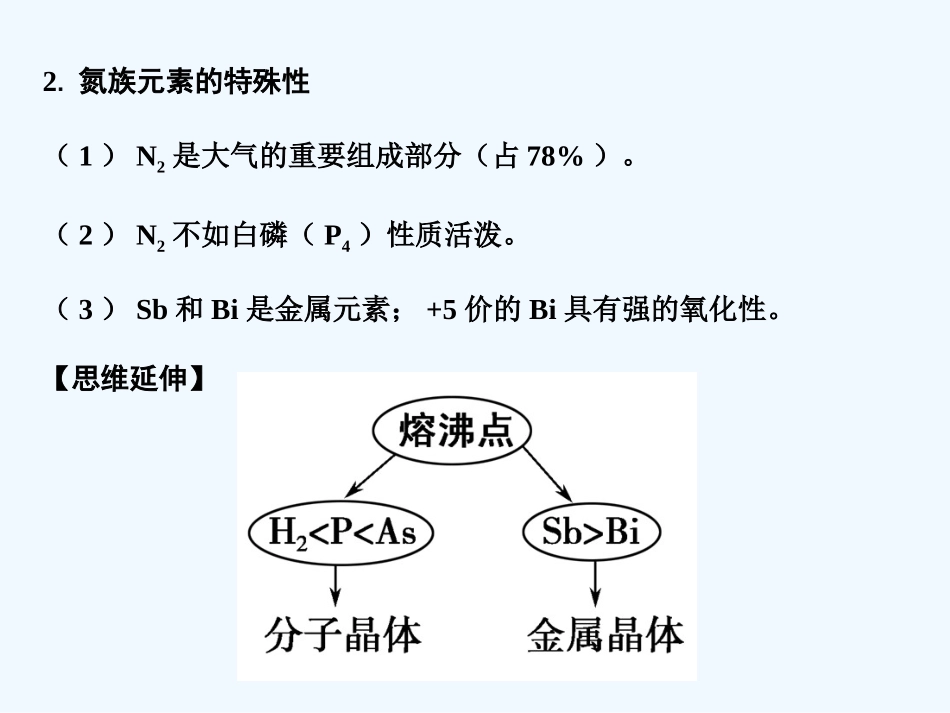
【思维延伸】知识点2氮气N2(无色、难溶于水、难液化的气体)问题2:为什么经常用N2作保护气
它有什么特性
(1)结构特点氮分子是双原子分子,电子式为:NN:,结构式为NN,两个氮原子通过3个共价键结合起来,键能很大,所以N2很稳定
(2)化学性质由于氮分子的键能很大,所以氮气的性质很稳定,只在高温条件下才能发生一些化学反应
①与H2的反应:N2+3H22NH3;②与O2的反应:N2+O22NO;③与Mg的反应:3Mg+N2Mg3N2
点燃放电(3)氮的固定将游离态的氮转变为化合态的氮的过程叫氮的固定
氮的固定方式有自然固氮和人工固氮
如工业合成氨为人工固氮,雷雨天产生NO气体就属于自然固氮
(4)氮气的用途①惰性之用:保护气(充填灯泡、焊接金属,保存粮食等)
②作原料用:合成氨、制HNO3等
4.氮气及氮的化合物之间的转化(1)氮元素有+1,+2,+3,+4,+5等五种正价态,五种正价对应六种氧化物:N2O、NO、N2O3、NO2、N2O4、N2O5
其中N2O3和33N2O5分别是HNO2和HNO3的酸酐
NO是一种无色、还原性较强的气体,易被O2氧化为NO2
NO2是一种红棕色的、易溶于水与水反应的气体,氧化性强,能氧化SO2,能使湿润的KI淀粉试纸变蓝色