化学化学元素周期表和元素周期律的应用化学了解元素周期表中金属元素、非金属元素的简单分区
认识元素周期表是元素周期律的具体体现
体会元素周期表和元素周期律在科学研究和工农业生产中的指导意义
1234理解位置决定结构、结构决定性质、性质决定用途的化学思想
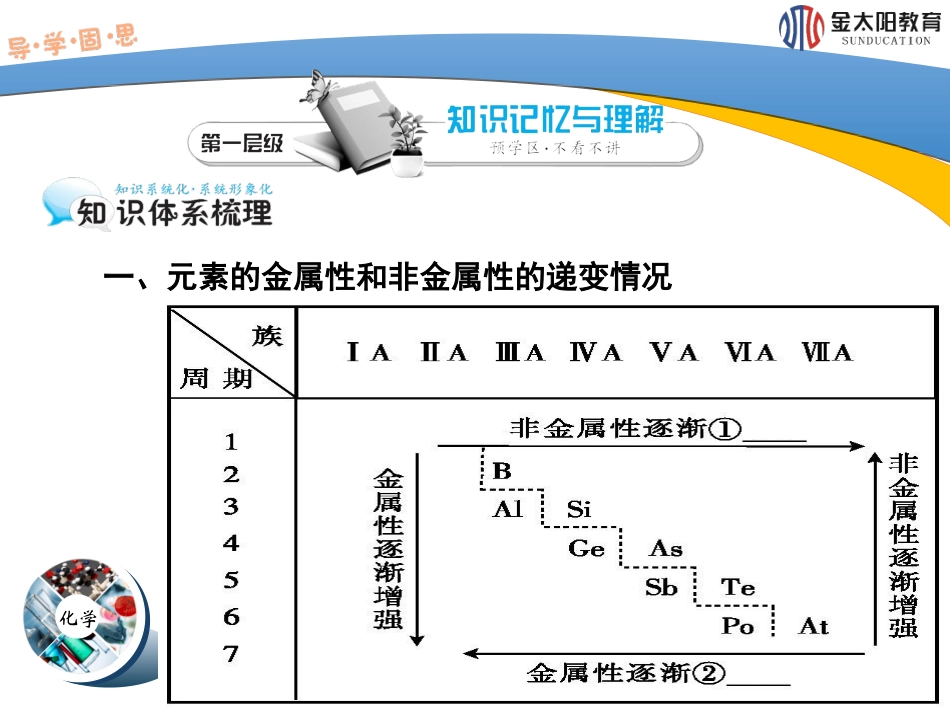
化学一、元素的金属性和非金属性的递变情况化学位于虚线附近的元素往往具有⑦_____性
上表中虚线上方和下方分别是⑤__________元素和⑥_______元素
非金属1由上表可以看出,元素周期表中非金属性、金属性最强的元素(不包括放射性元素)分别是③___、④___元素
金属2两FCs3化学(1)最低负价=⑨________-8;(2)最高正价+|最低负价|=8
通过上面的规律可以判断,“氢元素的最高正价为+1,最低负价为-7”是⑩______的,原因是____________________________________________________________________________
1主族元素:最高正价=最外层电子数(价电子数)=⑧__________
非金属主族元素,化合价的一般规律如下:二、元素常见化合价与元素在周期表中位置的关系主族序数错误主族序数氢为第一周期元素,最外层为2个电子时就达到了稳定结构,故氢元素的最低负价为-12化学1便于对元素性质进行系统研究
三、元素周期表和元素周期律的应用金属与非金属的分界过渡元素右上角2为发现新元素及预测它们的原子结构和性质提供了线索
3在周期表___________________中处寻找半导体材料
4农药中含有的As、F、Cl、S、P等元素集中在周期表_______区域
5在__________中寻找催化剂和耐高温、耐腐蚀的合金材料
化学1~20号元素中,非金属性最强的元素形成的单质是什么
金属性最强的元素形成的单质是什么
原子半径最小的是什么元素