1.基态原子核外电子排布(鲍林近似能级图)2.原子的成键特征与分子构型关系sp杂化:直线形(如BeCl2、HgCl2);sp2杂化:平面三角形(如BF3、BCl3);sp3杂化:四面体形(如CH4、CCl4)、三角锥形(如NH3)、V形(如H2O)
3.Cu与Cr原子的电子排布式本章重点提示1.σ键和π键的区别从轨道重叠方式来看可分为σ键和π键,σ键是指原子轨道以“头碰头”^方式相互重叠导致电子在核间出现的概率增大而形成的共价键;π键是指原子轨道以“肩并肩”方式相互重叠导致电子在核间出现的概率增大而形成的共价键
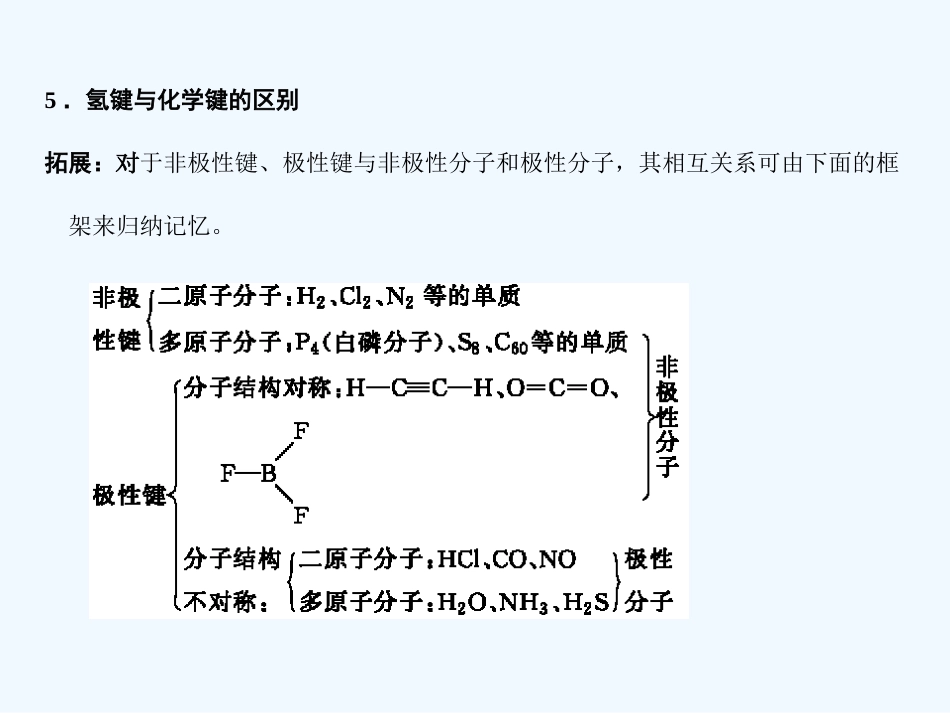
2.极性键和非极性键的区别3.共价键的极性与分子极性关系4.元素的电离能与电负性的区别5.氢键与化学键的区别拓展:对于非极性键、极性键与非极性分子和极性分子,其相互关系可由下面的框架来归纳记忆
1.晶体熔、沸点遵循下列规律晶体的结构特点决定了它的物理性质
当我们见到一组物体要比较它们的熔沸点大小时,应遵循以下分析顺序:(1)划分晶体类型
一般来说,晶体熔沸点大小顺序为:原子晶体>离子晶体>分子晶体
金属晶体比较复杂,要根据具体物质
(2)都是原子晶体,比较键长,键长越短,键能越大,熔沸点越高
如金刚石和晶体硅,由于金刚石的键长小于晶体硅的键长,金刚石的熔沸点比晶体硅的熔沸点高
(3)都是离子晶体,比较微粒间距离和离子所带电荷数,微粒间距离越小,键能越大,熔沸点越高;离子所带电荷数越多,熔沸点越高
NaCl比CsCl熔沸点高
(4)都是分子晶体,首先看是否存在氢键,相对分子质量相差不大的,存在氢键的熔沸点较高
如不存在氢键,则比较相对分子质量,相对分子质量越大,范德华力越大,熔沸点越高
(5)都是金属晶体,比较金属离子半径和离子所带电荷数,金属离子半径越大,熔沸点越低,所带电荷数越多,熔沸点越高
以上为理论推导,实际可能有特殊情况,故应根据实际情况再进行验证