第二节离子反应(第一课时)课本课本PP3030第第22、、33段段课本课本PP3030第第22、、33段段为什么NaCl溶液等能产生自由移动的离子
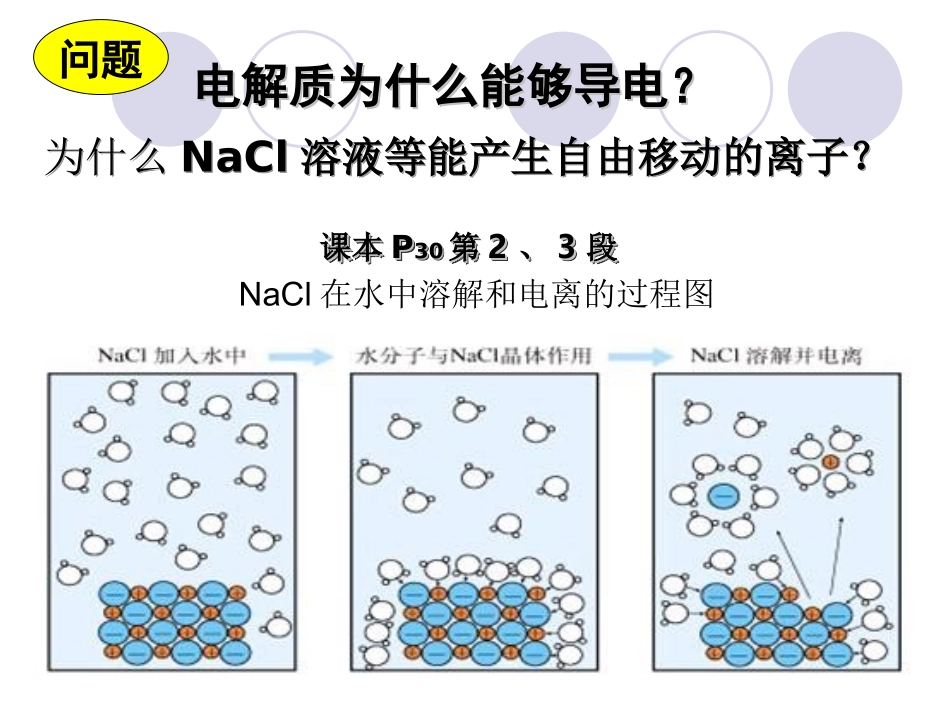
为什么NaCl溶液等能产生自由移动的离子
NaCl在水中溶解和电离的过程图问题电解质为什么能够导电
电解质为什么能够导电
电解质和非电解质一
酸、碱、盐在水溶液中的电离⑵非电解质:在水溶液里和熔融状态都不能导电的化合物
包括:绝大多数有机物、非金属氧化物、NH3⑴电解质:在水溶液里或熔融状态中能导电的化合物包括:酸、碱、盐、水、金属氧化物①电解质应该是化合物
如:铜(单质),氢氧化钠溶液(混合物)不是电解质②电解质的导电条件:水溶液或熔融状态
如:硫酸钡虽然其水溶液几乎不导电,但在熔化状态下能导电,因此它是电解质
③电解质导电必须是化合物本身能电离出自由移动的离子,而不是发生化学反应的生成物
如:CO2水溶液能导电,是由于CO2与水反应生成了H2CO3,所以CO2不是电解质
注意:一些不溶于水的盐,如一些不溶于水的盐,如BaSOBaSO44、、CaCOCaCO33等,是否为强电解质
等,是否为强电解质
((11)强电解质:全部电离成离子的电解质)强电解质:全部电离成离子的电解质2
强电解质和弱电解质强电解质和弱电解质问题包括:强酸(HCl、H2SO4、HNO3等)强碱(NaOH、KOH、Ca(OH)2、Ba(OH)2等)大多数的盐及金属氧化物⑵⑵弱电解质:只有部分电离成离子的电解质只有部分电离成离子的电解质包括::弱酸:(弱酸:(HH22COCO33、、CHCH33COOHCOOH等)等)弱碱弱碱[NH[NH33·H·H22OO、、Fe(OH)Fe(OH)33、、Cu(OH)Cu(OH)22等等]]水水结论:结论:1
相同条件下,不同种类的酸、碱、相同条件下,不同种类的酸、碱、盐的导电能力不同
盐的导电能力不同