第二节水的电离和溶液的酸碱性水的电离溶液的酸碱性和pH1:水的电离.水是一种_____的电解质
能发生_____电离
其电离方程式为:___________________简写___________________
极弱10-7H2O+H2OH3O++OH-微弱一、水的电离10-725℃时实验测得,在室温下1LH2O(即mol)中只有1×10-7molH2O电离,常温下纯水中c(H+)=______mol/L,c(OH-)=______mol/L
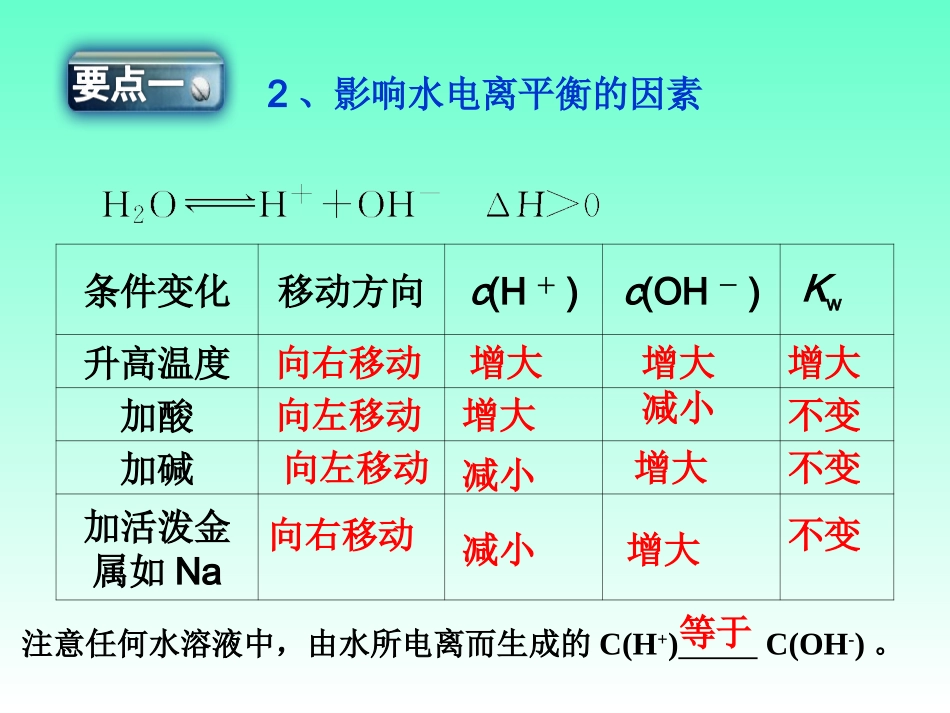
62、影响水电离平衡的因素条件变化移动方向c(H+)c(OH-)Kw升高温度加酸加碱加活泼金属如Na向右移动增大增大增大向左移动增大减小不变向左移动减小增大不变向右移动减小增大不变注意任何水溶液中,由水所电离而生成的C(H+)C(OH-)
等于1.在某温度时,测得纯水中的c(H+)=2
0×10-7mol·L-1,则c(OH-)为()A.2
0×10-7mol·L-1B.0
1×10-7mol·L-1C.1
0×10-14mol·L-1D.无法确定A2.在25℃时,测得某酸溶液中由水电离出来的c(OH-)=1
0×10-10mol·L-1,则由水电离出来的c(OH-)c(H+)为()A.1
0×10-7mol·L-1B.1
0×10-10mol·L-1C.1
0×10-20mol2·L-2D.无法确定[反馈练习]:Cc(H+)·c(OH-)3.水的离子积常数(1)水的电离平衡常数:K电离=_________________________
c(H2O)c(H+)·c(OH-)K电离c(H2O)(2)水的离子积常数水的离子积Kw=_______________=__________(1)Kw与化学平衡常数一样,其变化只受______的影响
在25℃时,c(H+)=c(OH-)=______mol/L,故此温度下Kw=_____