扬中市第二高级中学教学案高三年级化学备课组备课时间:2012
9专题九氧化还原反应(1)氧化还原方程式的书写一、高锰酸钾与一些还原剂的反应1、高锰酸钾溶液是强氧化剂,通常用酸化,不用盐酸酸化的理由是(用离子方程式表示)2、请写出酸性高锰酸钾溶液分别与双氧水、SO2、乙烯反应的离子方程式:【小结】高锰酸钾在水溶液中还原产物的价态为,以存在于水溶液中
K2Cr2O7也是强氧化剂,请写出酸性K2Cr2O7溶液分别与双氧水、浓盐酸的离子方程式:写出Cr2O72—与FeSO4溶液在酸性条件下生成Cr3+反应
二、双氧水作氧化剂参与的反应双氧水有绿色氧化剂之称,无污染,且不会引入新杂质
请写出下列反应的离子方程式
在酸性条件下,双氧水与Fe2+反应:双氧水与SO2反应:在酸性条件下,双氧水与I-反应:双氧水与亚硫酸钠反应:酸性条件下,SnSO4还可以用作双氧水去除剂,反应:碱性条件下,30%H2O2氧化CrO2-生成CrO42-反应:
【小结】双氧水的还原产物价态为,一般为
三、归中反应归中规律:同一元素不同价态原子间发生氧化还原反应,通常有下面几种情况,你认为不可能发生的是____
【小结】由此得出的归中规律是__________
【练习】写出下列反应的离子方程式或化学方程式:KClO3与浓盐酸反应:在酸性条件下,KIO3与KI反应:SO2与H2S的反应:亚硫酸钠与硫化钠在酸性条件下反应:浓硫酸与单质硫的反应:氨气与NO2反应:四、歧化反应氯气与氢氧化钠反应:单质硫与氢氧化钠反应:1扬中市第二高级中学教学案高三年级化学备课组备课时间:2012
9NO2与水反应:【总结】氧化还原方程式的书写,先结合反应的环境和价态变化规律写出氧化产物和还原产物后,再写其他产物,再依据电子守恒、电荷守恒和原子守恒配平,检查
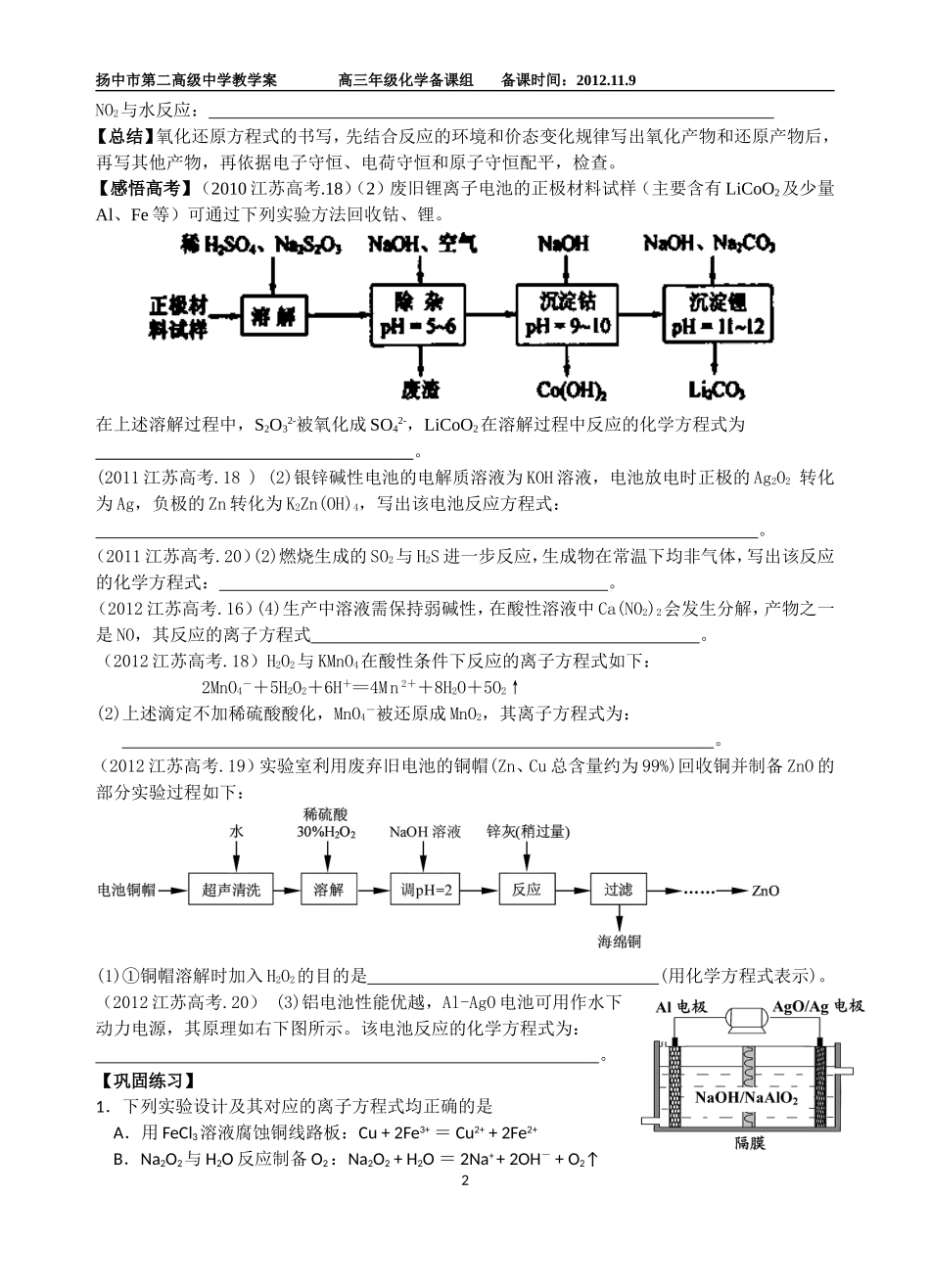
【感悟高考】(2010江苏高考
18)(2)废旧锂离子电池的正极材料