第1课时:物质的量的单位——摩尔1、了解物质的量及其单位---摩尔,了解物质的量与微观粒子数之间的关系
2、了解摩尔质量的概念
3、了解物质的量、摩尔质量、物质质量之间的关系
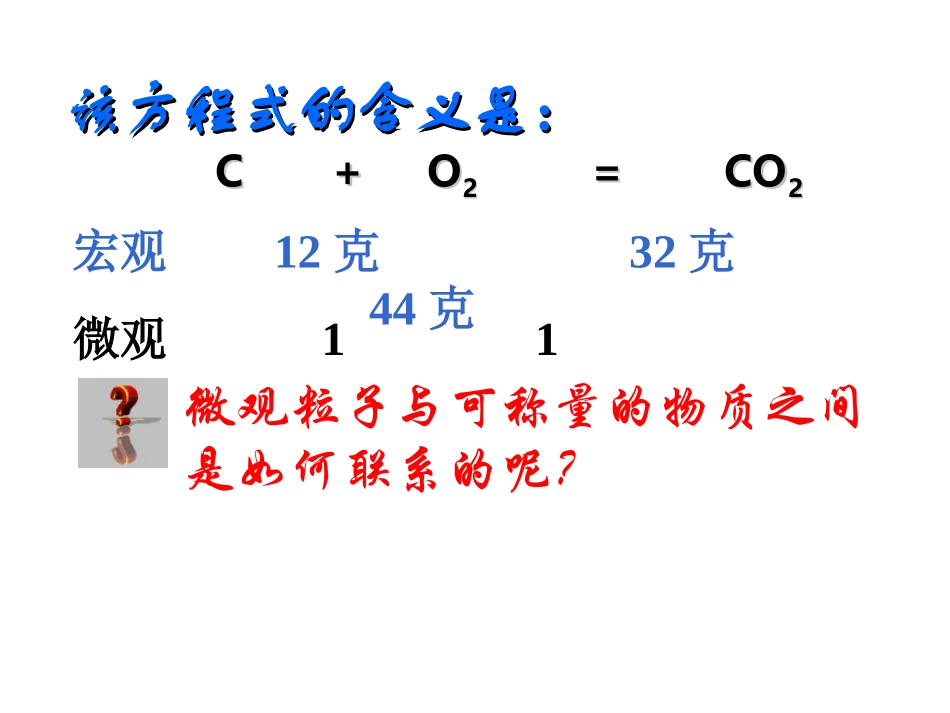
该方程式的含义是:该方程式的含义是:C+OC+O22=CO=CO22宏观12克32克44克微观111微观粒子与可称量的物质之间是如何联系的呢
例:12克12C中含有多少个碳原子
一个碳原子的质量:1
99×10-23克所以,12克/1
99×10-23克≈6
02×1023如此巨大的数字不方便计算和交流,怎么办
02×1023个直径为2
5cm的硬币排成一行(展示硬币),可以来回于地球与太阳之间240
如果把6.02×1023粒米给全球60亿人吃,每人每天吃一斤,要吃1414万年万年
想办法在分子数和质量之间找到一个桥梁——集体单位
箱方便计量瓶24瓶设立与“箱”、“班”类似的数量集体来描述数量多少班学生人数60人左右化学物质微粒个数数量巨大,为了方便计量,1瓶1箱=24瓶物质的量表示含有一定数目粒子的集合体(常用集合体(常用11mol衡量))物质的量一、一箱啤酒一打铅笔一双筷子一盒别针碳原子数单位是摩尔、简称摩,符号:mol1打铅笔1双筷子1箱啤酒1盒别针宏观物质微观粒子1mol分子、离子、原子……把微小物质扩大倍数形成一定数目的集体以便于方便生活、方便科学研究、方便相互交流物质的量是表示含有一定数目粒子的集合体集合体的物理量1、是国际单位制七个基本物理量之一2、物质的量的单位是摩尔、简称摩,符号:molC、用摩尔为单位表示某物质的物质的量时,必须指明物质微粒的名称、符号或化学式
如:1molH、1molH+、1molH2,不能用“1mol氢”这样含糊无意义的表示
3、注意事项:A、“物质的量”是一个物理量的全称,是一个专有名词;物质的量不能当成物质的数量或质量来理解