(2)【典例1】(江苏高考命题研究专家原创卷三)现有一瓶实验室放置已久的可能变质的Na2O2固体,为了研究它的组成,请你参与同学们进行的如下探究活动:可选用的试剂:浓硫酸、浓硝酸、稀盐酸、澄清石灰水、蒸馏水、品红溶液、火柴;仪器自选
(1)提出假设假设一:固体全部是Na2O2;假设二:固体全部是Na2CO3;假设三:____________________________
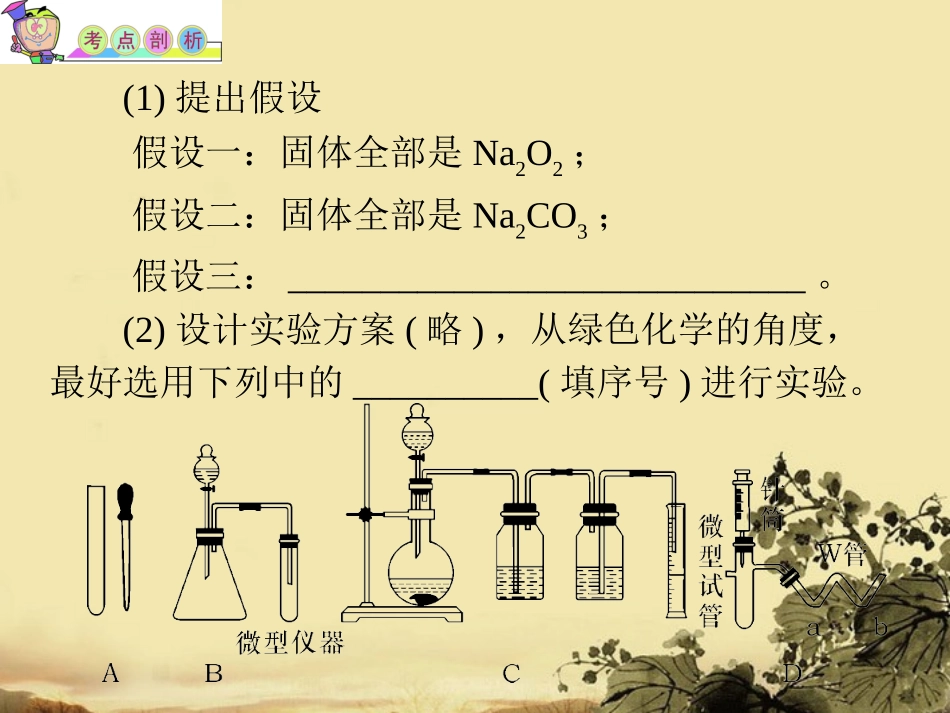
(2)设计实验方案(略),从绿色化学的角度,最好选用下列中的__________(填序号)进行实验
(3)进行实验:请在下表中用简要文字写出实验步骤、预期现象和结论
实验步骤预期现象和结论步骤1:步骤2:……(1)Na2O2吸收空气中的二氧化碳转变为白色的Na2CO3固体,第三种假设是部分变质,即既有Na2O2又有Na2CO3
(2)本题的设计方案较多,但结合题给药品和绿色化学的要求,应进行微型化设计,避免大量的废弃药品污染环境,故选择D装置
(3)本题要根据所给药品进行合理的步骤设计,既要检测有没有产物二氧化碳,又要检测有没有产物氧气,从而确定哪一种假设是正确的
【解析】(3)如下表格实验步骤预期现象和结论步骤1:取适量固体样品于微型试管中;在W管a处滴入澄清石灰水,b处滴入浓硫酸;用胶管将W管与微型试管连接好步骤2:用针筒吸入稀盐酸,将针头穿过微型试管的胶塞,向固体中注入过量盐酸,在W管尾部插入带火星的火柴有气泡放出,若a处澄清石灰水不变浑浊,火柴复燃则假设一正确;若a处澄清石灰水变浑浊但火柴不复燃,则假设二正确;若a处澄清石灰水变浑浊且火柴复燃,则假设三正确答案:(1)固体中既有Na2O2,又有Na2CO3(2)D【迁移训练1】(江苏高考命题研究专家原创五)实验室中有两瓶失去标签的中学常见药品,一瓶是固体(单一成分),另一瓶是无色液体,某同学取少量两种药品在试管中混合,立即产生一种无色气体