(2009年高考二轮专题复习)【学习目标】1、掌握原电池、电解池的概念及原理,了解铜的电解精炼、镀铜、氯碱工业反应原理2、学会电极的判断,学会正确书写电极反应及总反应方程式,掌握常见离子放电的规律;3、能运用得失电子守恒法解决电化学的相关计算
高考化学二轮专题《电化学》复习高考化学二轮专题《电化学》复习【复习重点】原电池、电解原理及应用;电极反应方程式书写【知识概括】一个反应:氧化还原反应一个计算:得失电子守恒法解决电化学的相关计算两个转化:化学能和电能的相互转化两个应用:原电池原理应用、电解原理应用三个条件:原电池、电解池的形成条件四个池子:原电池、电解池、电镀池、电解精炼池【专题难点】电极反应及总反应方程式正确书写一、原电池、电解池工作原理一、原电池、电解池工作原理1
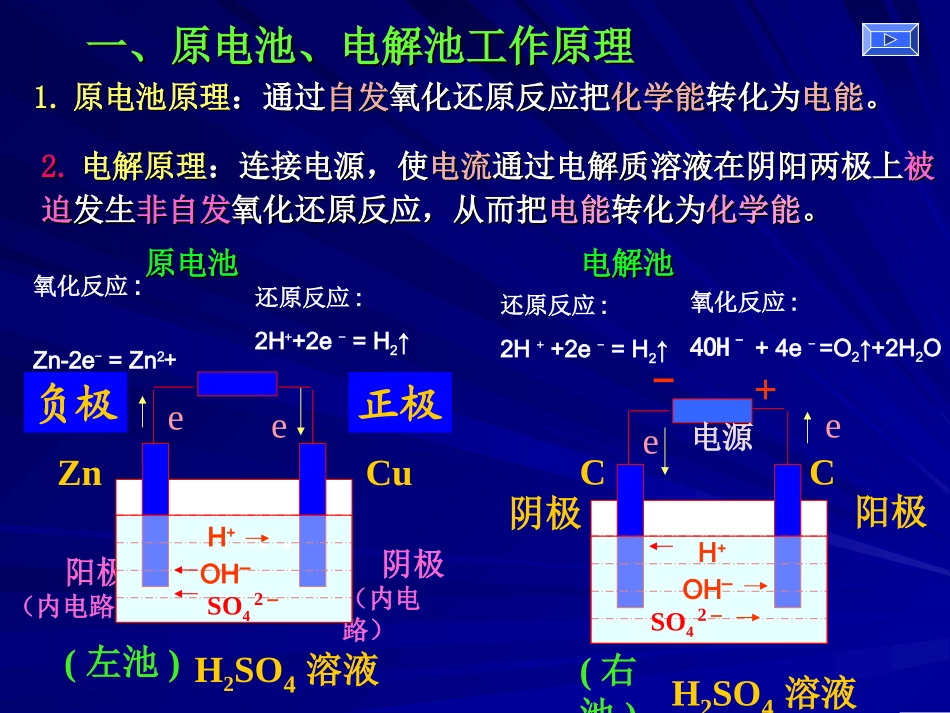
原电池原理原电池原理:通过:通过自发自发氧化还原反应把氧化还原反应把化学能化学能转化为转化为电能电能
电解原理电解原理:连接电源,使:连接电源,使电流电流通过电解质溶液在阴阳两极上通过电解质溶液在阴阳两极上被被迫迫发生发生非自发非自发氧化还原反应,从而把氧化还原反应,从而把电能电能转化为转化为化学能化学能
阳极(内电路)阴极(内电路)CCH2SO4溶液阳极阴极+-ee电源正极负极CuZnH2SO4溶液eeH+SO42–H+SO42–氧化反应:Zn-2e-=Zn2+还原反应:2H++2e-=H2↑还原反应:2H++2e-=H2↑氧化反应:4OH–+4e-=O2↑+2H2O(左池)(右池)原电池原电池电解池电解池OH–OH–原电池原电池电解池电解池定义定义((能量转能量转化化))化学能转变成电能的装置
化学能转变成电能的装置
将电能转变成化学能的装置
将电能转变成化学能的装置
形成形成条件条件①①活动性不同两电极活动性不同两电极((燃料电池燃料电池电极电极除外除外))②②电解质溶液电解质溶液(