高二化学(选修)化学反应原理专题1第一单元化学反应中的热效应(第一课时化学反应的焓变)【学习目标】1.了解反应热和焓变的含义
2.理解放热反应和吸热反应的实质,理解化学反应过程中能量变化的原因
3.熟练书写热化学方程式,并利用热化学方程式进行简单计算
【重点难点】热化学方程式的书写及利用热化学方程式进行简单计算
学习过程:化学反应过程中既有变化,又有变化
是化学变化中能量变化的主要形式之一
一、化学反应的焓变1.反应热在化学反应过程中,当反应物和生成物具有相同时,所或的热量
2.焓变在的条件下,化学反应过程中或的热量
符号,常用单位
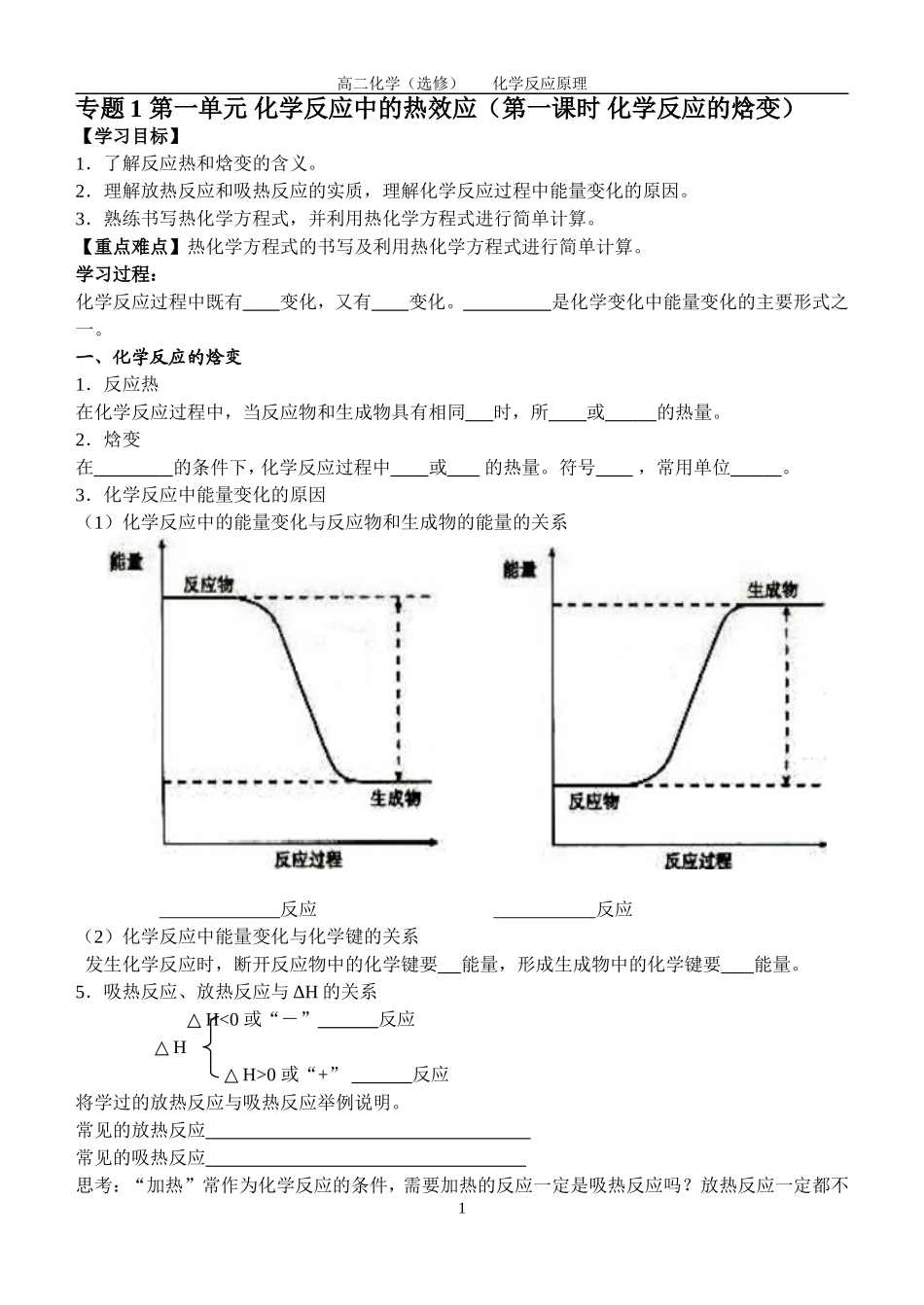
3.化学反应中能量变化的原因(1)化学反应中的能量变化与反应物和生成物的能量的关系反应反应(2)化学反应中能量变化与化学键的关系发生化学反应时,断开反应物中的化学键要能量,形成生成物中的化学键要能量
5.吸热反应、放热反应与ΔH的关系H0△或“+”反应将学过的放热反应与吸热反应举例说明
常见的放热反应常见的吸热反应思考:“加热”常作为化学反应的条件,需要加热的反应一定是吸热反应吗
放热反应一定都不1高二化学(选修)化学反应原理需要加热吗
二、热化学方程式【交流与讨论】观察下列表示在25℃(298K)、101kPa下氢气在氧气中燃烧生成水的反应热的四个化学方程式,分析其在书写上与化学方程式有何不同①2H2(g)+O2(g)=2H2O(l)H(298K)=△–571
6kJ•mol—1②2H2(g)+O2(g)=2H2O(g)H(298K)=△–483
6kJ•mol—1③H2(g)+O2(g)=H2O(l)H(298K)=△–285
8kJ•mol—1④H2(g)+O2(g)=H2O(g)H(298K)=△–241
8kJ•mol—11.定义:能够表示的化学方程式
2.特点(1)指明了反应时的和,若在25℃、101kPa时进行的反应,可不注明