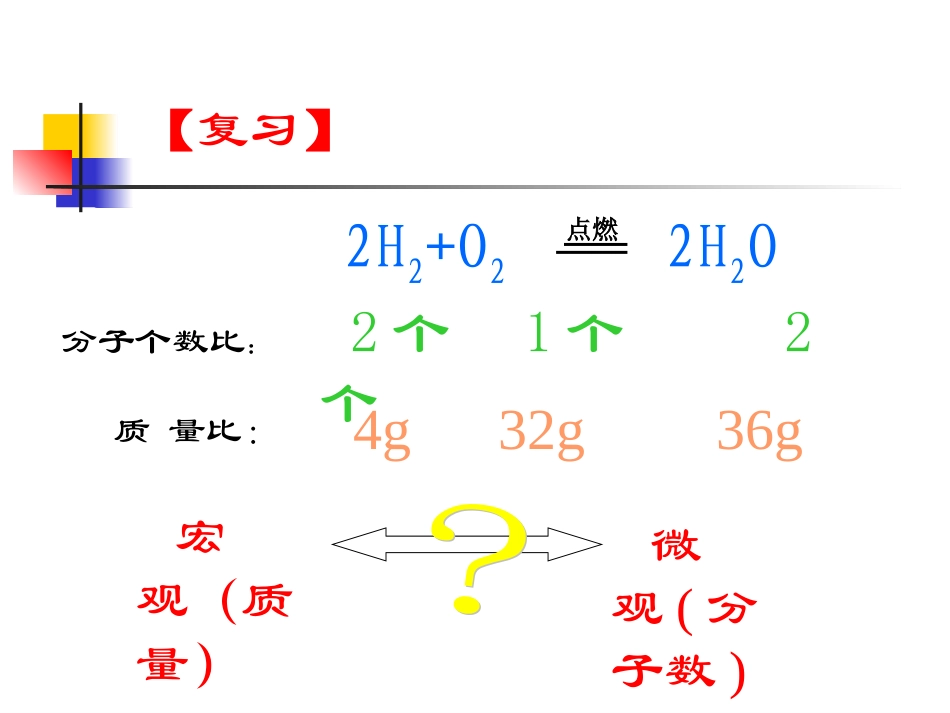
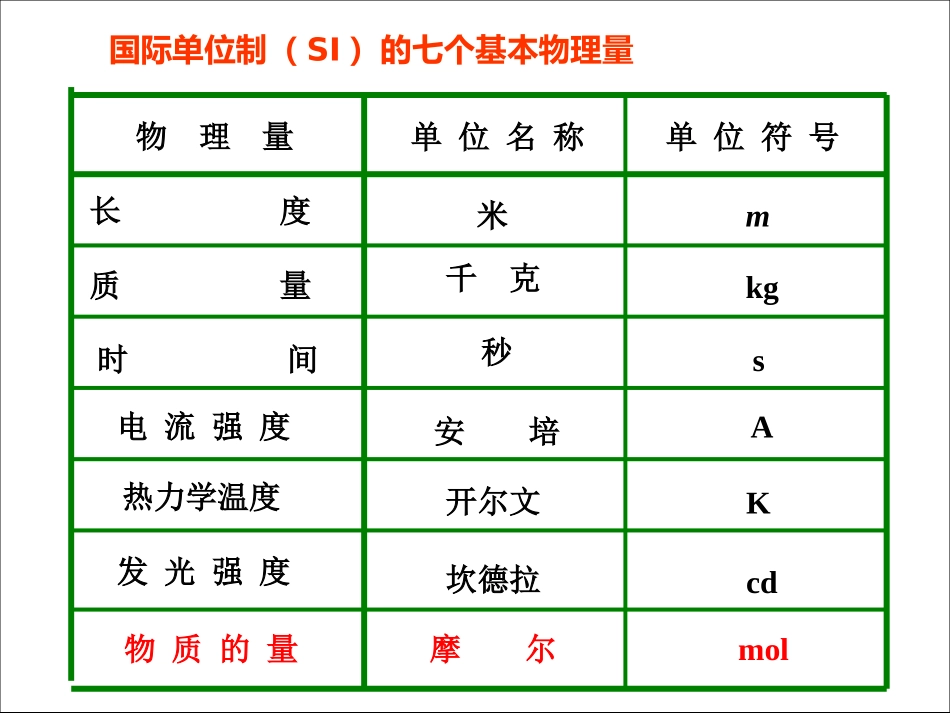
第二节化学计量在实验中的应用第一章从实验学化学【复习】2H2+O22H2O4g32g36g2个1个2个质量比:分子个数比:点燃宏观(质量)微观(分子数)物理量单位名称单位符号长度质量时间电流强度热力学温度发光强度米千克秒安培开尔文坎德拉摩尔mkgsAKcdmol国际单位制(SI)的七个基本物理量物质的量1
概念:是表示含有一定数目微观粒子的集合体
分子、原子、离子、电子、质子、中子等所有的微观粒子及它们的特定组合一、物质的量2
单位:摩尔(简称:摩)注意事项:1
物质的量是一个专用名词,不能理解为“物质的质量”、“物质的数量”、“物质量”
物质的量只适用于微观粒子只适用于微观粒子,不适用于宏观物质
用“摩尔”表示物质的量时,应用化学式具体指明粒子的种类指明粒子的种类
1mol苹果2
1mol氧气判断:3
1mol氢4
1molH25
1molH4
摩尔的数值可以是整数,也可以是小数可以是整数,也可以是小数
对于化学式表示微观粒子或它们的特定组合,还应明确微粒间微观粒子或它们的特定组合,还应明确微粒间的内在联系的内在联系
1molNO7
5molH2填空:8
1molMgCl2中含有molMg2+和molCl-;9
3molNH3中含有molN和molH;二、物质的量的单位——摩尔1
概念:1mol粒子集体所含的粒子数与0
012kg12C所含的碳原子数相同
思考一:1摩尔物质的标准是多少呢
012kg12C所含的碳原子数是多少呢
单位符号:mol把1mol任何粒子的粒子数叫做阿伏加德罗常数思考三:阿伏加德罗常数与6
021023个碳原子数的关系是多少呢
三、阿伏加德罗常数1
概念:1mol任何粒子的粒子数2
符号:NA3
单位:个mol-1简写成:mol-14
数值:约为6
021023mol-15