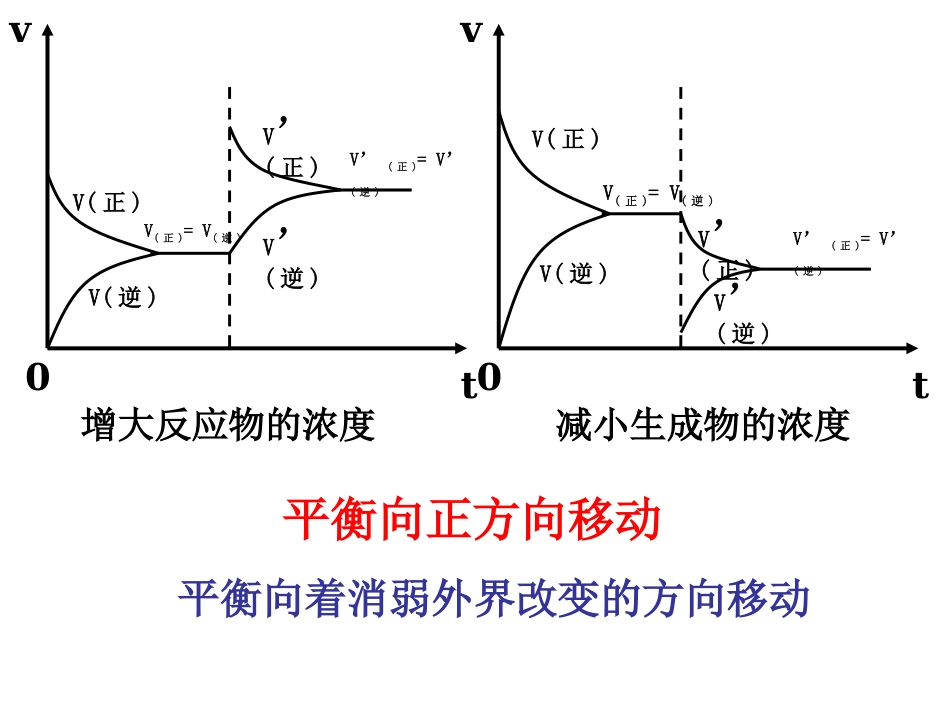
其他条件不变,改变影响平衡的外界条件(浓度、温度、压强),平衡将向着消弱外界改变的方向移动一、化学平衡移动原理1、浓度对平衡的影响0vtV(正)V(逆)V(正)=V(逆)V’(正)V’(逆)V’(正)=V’(逆)减小生成物的浓度0vtV(正)V(逆)V(正)=V(逆)V’(正)V’(逆)V’(正)=V’(逆)增大反应物的浓度平衡向正方向移动平衡向着消弱外界改变的方向移动0vtV(正)V(逆)V(正)=V(逆)V’(逆)V’(正)V’(正)=V’(逆)增大生成物的浓度0vtV(正)V(逆)V(正)=V(逆)V’(逆)V’(正)V’(正)=V’(逆)减小反应物的浓度平衡向逆方向移动平衡向着消弱外界改变的方向移动2、压强对平衡的影响平衡的移动与反应前后气体分子个数有关V(正)原平衡V’V’新平衡vt反应前后气体分子个数改变的反应增大压强,平衡向气体分子个数减小方向移动平衡向着消弱外界改变的方向移动V’0vV(正)V’V(逆)新平衡反应前后气体分子个数改变的反应减小压强,平衡向气体分子个数增大方向移动平衡向着消弱外界改变的方向移动v原平衡V’新平衡t反应前后气体分子个数不发生改变的反应改变压强,平衡不发生移动v原平衡V’新平衡t3、温度对平衡的影响平衡的移动与反应的热效应有关vt原平衡V’V’升高温度,平衡向吸热方向移动平衡向着消弱外界改变的方向移动V’0vV(正)V’V(逆)新平衡降低温度,平衡向放热热方向移动平衡向着消弱外界改变的方向移动v原平衡V’新平衡t催化剂对平衡移动无影响二、化学平衡移动原理的应用工业上对于一些可逆反应,选择适当的条件,增大反应的速率和反应物的转化率,提高产量合成氨工业条件的选择合成氨工业条件的选择NN22(g)+3H(g)+3H22(g)2NH(g)2NH33(g)(g)△△HH==-92
4kJ·mol-92
4kJ·mol--11⑴⑴、注入过量、注