第二节影响化学反应速率的因素影响反应速率的因素(2)外部因素:(1)内部因素(主要因素):决定化学反应速率的因素是参加反应的物质本身的化学性质
①浓度,②压强,③温度,④催化剂,⑤其他因素:光、固体颗粒表面积、反应物的状态、原电池原理等
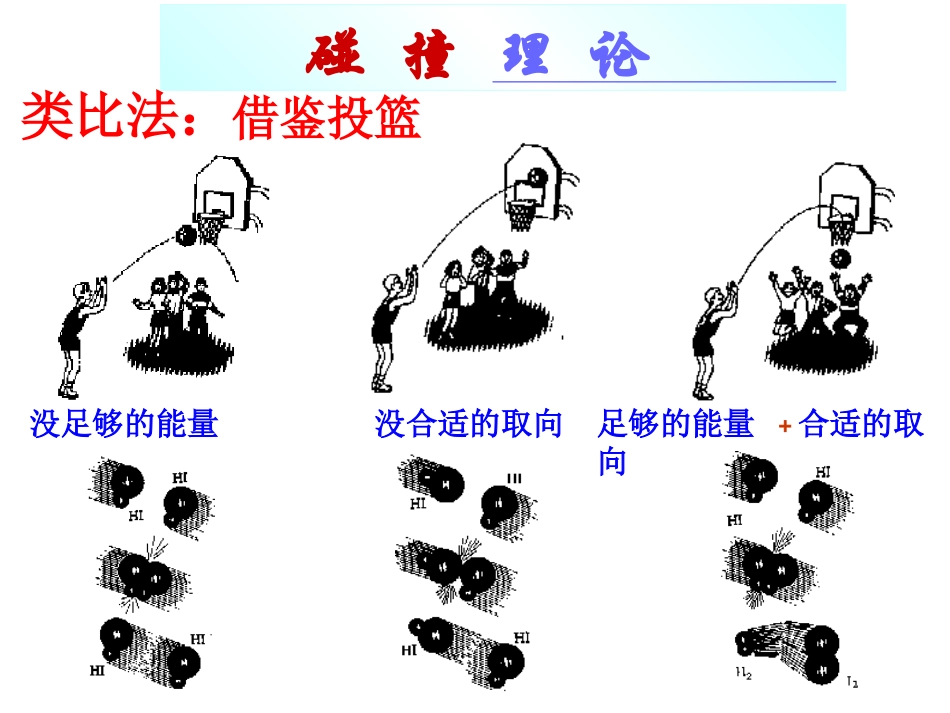
复习:没合适的取向没足够的能量足够的能量+合适的取向类比法:借鉴投篮碰撞理论能够发生化学反应的碰撞
有可能发生有效碰撞的分子
活化分子所多出普通分子的那部分能量E1
(即活化分子能量与反应物分子平均能量之差)有效碰撞:活化分子:活化能:n活=n总×活%活化分子百分数:(活化分子数/反应物分子数)×100%E1——表示活化能,E2——表示活化分子变成生成物分子释放的能量E2-E1——表示反应热有效碰撞次数越多,化学反应的速率就越大吗
反应速率越大单位时间单位体积有效碰撞次数越多单位体积活化分子数越多甲:一分钟有效碰撞100次乙:十分钟有效碰撞500次甲、乙相同条件下反应甲:整个容器中有效碰撞300次乙:半个容器中有效碰撞150次单位时间单位体积的有效碰撞次数又是由什么决定的呢
活化能的大小和反应速率有什么关系
活化能越低,单位体积内活化分子数越多,有效碰撞频率越大,化学反应速率就会越快
一个反应经历的过程一个反应经历的过程普通分子活化能活化分子合理取向的碰撞有效碰撞新物质能量一、浓度对反应速率的影响1、在其他条件不变时,增大反应物浓度,可以增大反应速率;减小反应物的浓度,可以减小化学反应的速率
实验2-2结论:浓度大的H2C2O4(aq)先褪色2KMnO4+5H2C2O4+3H2SO4==K2SO4+2MnSO4+10CO2↑+8H2O浓度对反应速率的影响本质原因在其他条件不变时,对某一反应来说,活化分子百分数是一定的,即单位体积内的活化分子数与反应物的浓度成正比
所以当反应物的浓度增大时,单位体积内的分子数增多,活化分子数也相应的增多,有效