离子晶体一、离子晶体1、定义:由阳离子和阴离子通过离子键结合而成的晶体
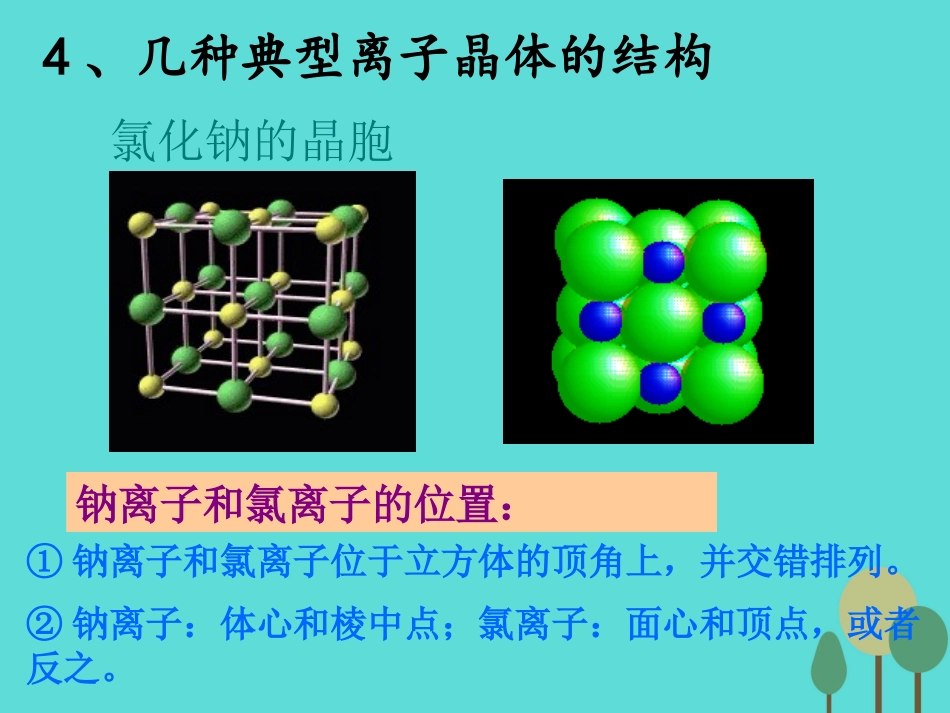
2、成键微粒:阴、阳离子3、物理性质:较高的熔点,较大的硬度固体不导电,熔融状态和水溶液中导电多数易溶于水,难溶于有机溶剂钠离子和氯离子的位置:①钠离子和氯离子位于立方体的顶角上,并交错排列
②钠离子:体心和棱中点;氯离子:面心和顶点,或者反之
氯化钠的晶胞4、几种典型离子晶体的结构分析思考:1、Na+配位数
Cl-配位数
离子晶体中的离子配位数(C.N.)离子周围最邻近的异电性离子的数目66钠离子周围最近且距离相等的氯离子可连接成正八面体2、与Na+等距离且最近的Na+各有几个
与Cl-等距离且最近的Cl-各有几个
3、每个晶胞含钠离子、氯离子的个数12个(2)氯化铯型晶胞---Cs+---Cl-CsCl的晶体结构及晶胞构示意图CsCl晶胞(1)铯离子和氯离子的位置:铯离子:体心氯离子:顶点;或者反之
(2)每个晶胞含铯离子、氯离子的个数铯离子:1个;氯离子:1个(3)铯离子、氯离子配位数各是多少
铯离子:8;氯离子:8(3)CaF2型晶胞①Ca2+的配位数:8②F-的配位数:4③一个CaF2晶胞中含:4个Ca2+和8个F-5、决定离子晶体结构的因素r+r-=r+r-=0
93NaCl型CsCl型(1)阳阴离子的半径比(几何因素)离子Na+Cs+Cl-离子半径(pm)95169181(2)阴阳离子的电荷比(电荷因素)阴阳离子的电荷比阴阳离子的个数比阴阳离子的配位数NaClCsClCaF2几何因素、电荷因素是决定晶体结构的重要因素1:11:16、61:11:18、81:22:18、4二、晶格能1、定义:拆开1mol离子晶体使之形成气态阴离子和气态氧离子时所吸收的能量单位:kJ/molNaFNaClNaBrNaIMgOCaOSrOBaO离子电荷11112222核间距/pm282298晶格能kJ/m