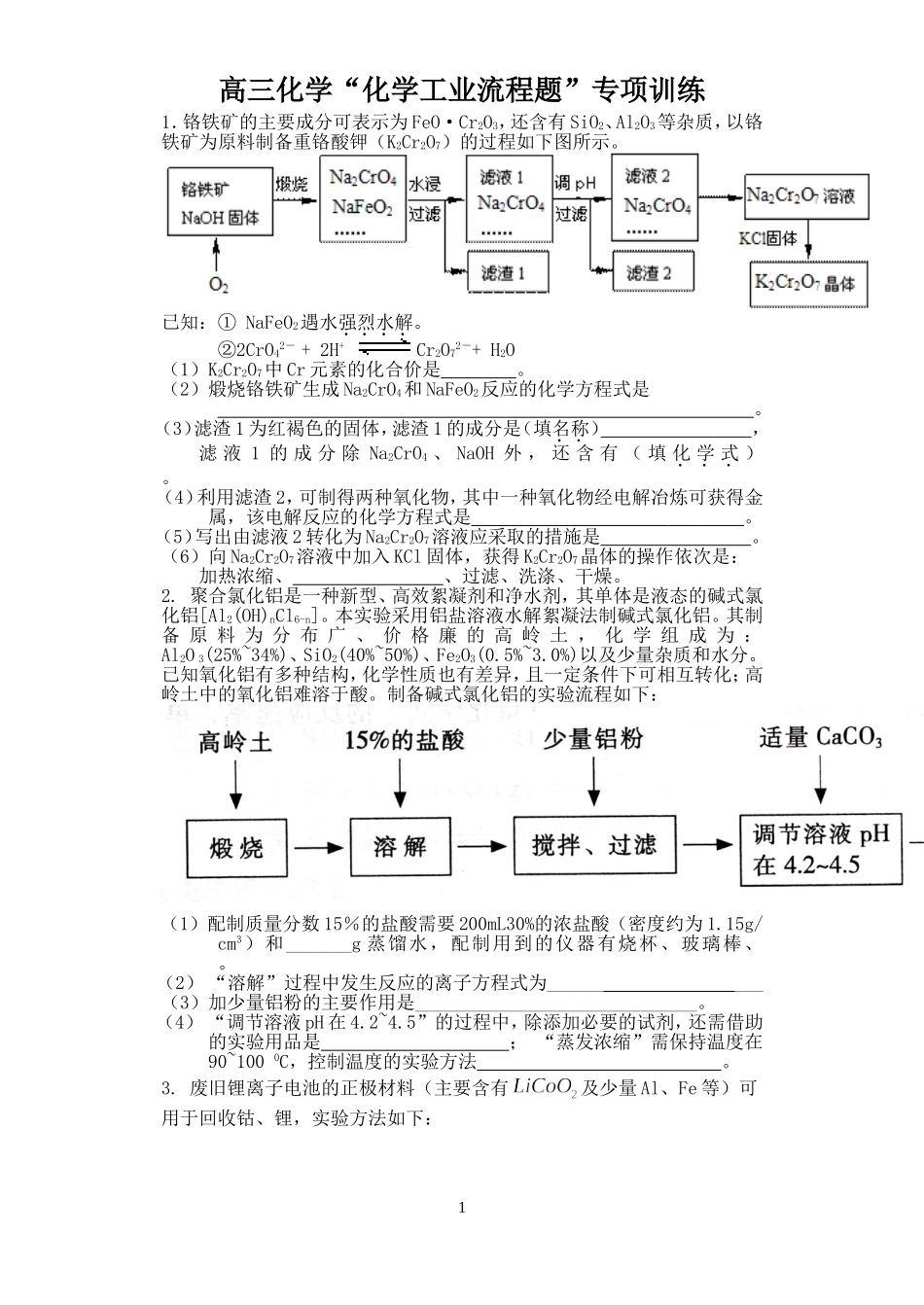
高三化学“化学工业流程题”专项训练1.铬铁矿的主要成分可表示为FeO·Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如下图所示
已知:①NaFeO2遇水强烈水解
②2CrO42-+2H+Cr2O72-+H2O(1)K2Cr2O7中Cr元素的化合价是
(2)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
(3)滤渣1为红褐色的固体,滤渣1的成分是(填名称),滤液1的成分除Na2CrO4、NaOH外,还含有(填化学式)
(4)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是
(5)写出由滤液2转化为Na2Cr2O7溶液应采取的措施是
(6)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、、过滤、洗涤、干燥
聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝[Al2(OH)nCl6-n]
本实验采用铝盐溶液水解絮凝法制碱式氯化铝
其制备原料为分布广、价格廉的高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0
0%)以及少量杂质和水分
已知氧化铝有多种结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸
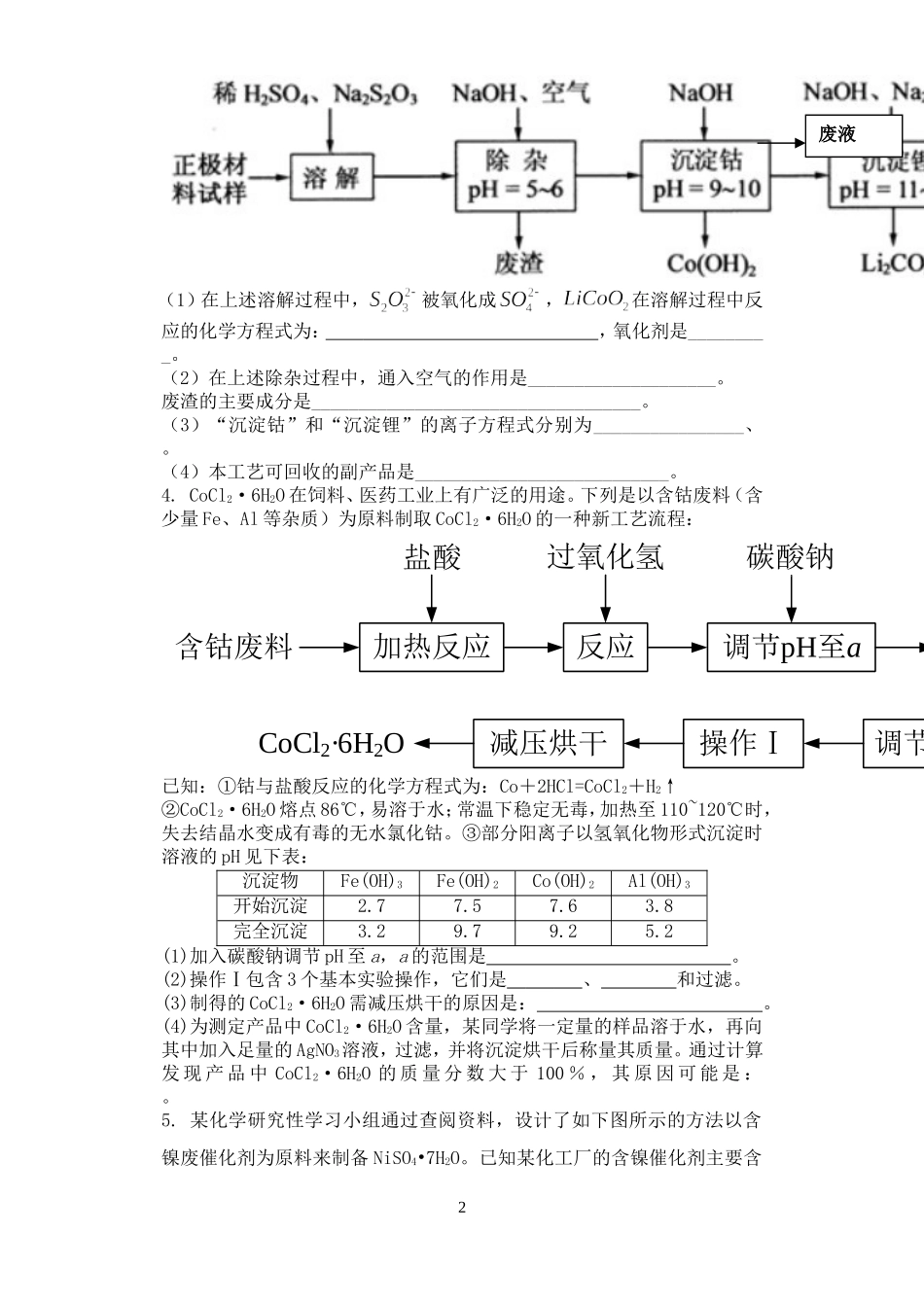
制备碱式氯化铝的实验流程如下:(1)配制质量分数15%的盐酸需要200mL30%的浓盐酸(密度约为1
15g/cm3)和_______g蒸馏水,配制用到的仪器有烧杯、玻璃棒、
(2)“溶解”过程中发生反应的离子方程式为_________(3)加少量铝粉的主要作用是______________________________
(4)“调节溶液pH在4
5”的过程中,除添加必要的试剂,还需借助的实验用品是;“蒸发浓缩”需保持温度在90~1000C