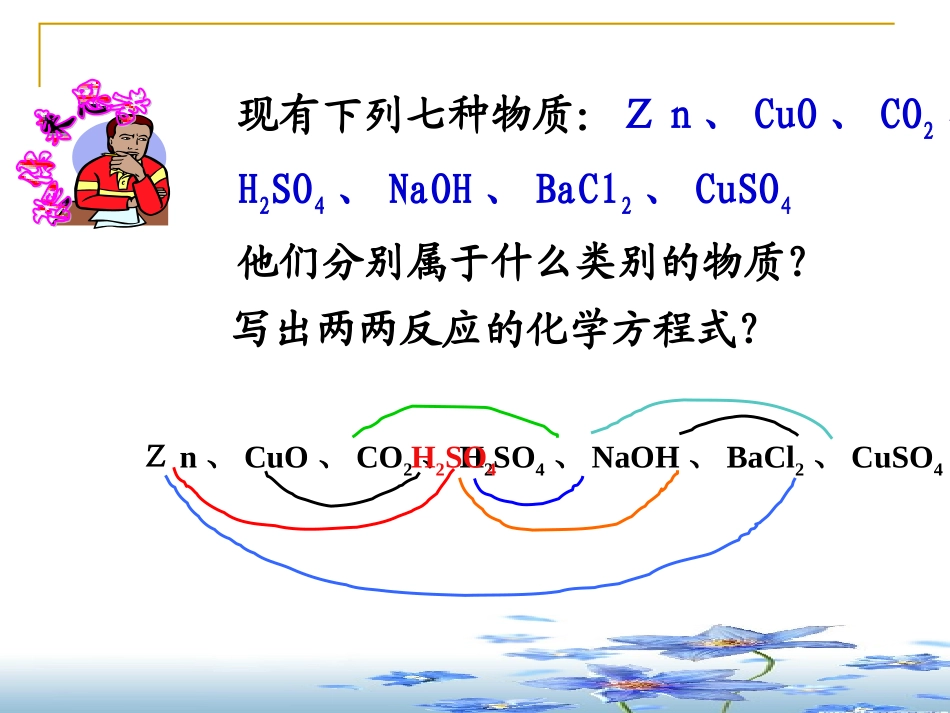
H、O、S、Na这四种元素任意组合能组成几种物质,写出相应的化学式
H2SO4、H2SO3H2、O2、O3、S、NaH2O、H2O2、H2S、SO2、SO3、Na2O、Na2SNa2SO4、Na2SO3、NaOHNaHSO4现有下列七种物质:Zn、CuO、CO2、H2SO4、NaOH、BaCl2、CuSO4他们分别属于什么类别的物质
Zn、CuO、CO2、H2SO4、NaOH、BaCl2、CuSO4H2SO4写出两两反应的化学方程式
Zn+CuSO4===ZnSO4+CuZn+H2SO4===ZnSO4+H2CuO+H2SO4===CuSO4+H2OCO2+2NaOH===Na2CO3+H2OH2SO4+2NaOH===Na2SO4+2H2OH2SO4+BaCl2===BaSO4+2HCl2NaOH+CuSO4===Cu(OH)2+Na2SO4BaCl2+CuSO4===CuCl2+BaSO41
跟酸反应的有哪几类物质
2.跟碱反应的有哪几类物质
3.跟盐反应的有哪几类物质
思考下列问题,完成任务单第二题4
请将能反应的两类物质用小短线“——”连接起来
酸碱盐的转化金属氧化物非金属氧化物酸碱盐盐金属判断下列化学方程式是否正确
Cu+2HClCuCl2+H22
Fe+2AgClFeCl2+2Ag3
2NaOH+CaCl22NaCl+Ca(OH)24
Na2CO3+CaCl2CaCO3+2NaCl一
位于氢前的金属能置换出盐酸、硫酸中的氢二
位于前面的金属能把位于后面的金属从它们的化合物的溶液中置换出来KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu金属活动性顺序由强逐渐减弱金属活动性顺序:主要应用:在金属活动性顺序中酸碱盐转化的规律:有沉淀、气体、水生成复分解反应才可以发生
活动性排在氢前面的金属才能与酸发生置换反应;活动性排在前面的金属才能把其后