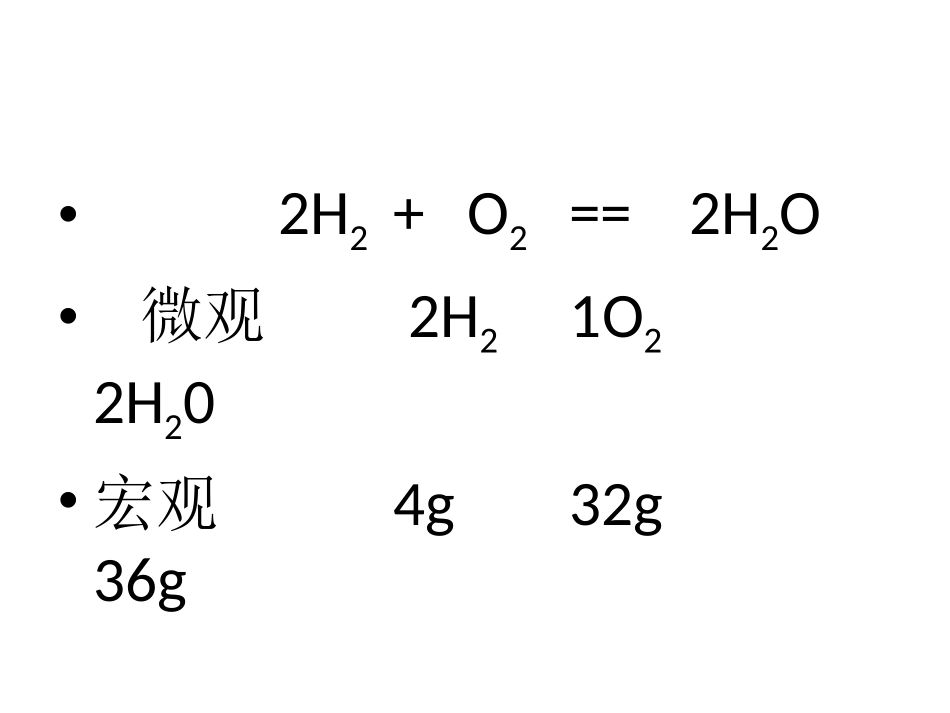
化学计量在实验中的应用物质的量的单位------摩尔•2H2+O2==2H2O•微观2H21O22H20•宏观4g32g36g物质的量是把微观粒子和宏观物质联系起来的一座桥梁
(难见、难称量)微观粒子宏观物质(可见、可称量)物质的量国际单位制的基本单位量的名称单位名称单位符号长度米m质量(重量)千克(公斤)kg时间秒s电流安[培]A热力学温度开[尔文]K物质的量摩[尔]mol发光强度坎[德拉]cd物质的量的单位—摩尔1
物质的量:⑴概念:物质的量是一种基本物理量,它表示含有一定数目粒子的集体,符号为n,单位为mol
“物质的量”是一个专用名词,不能拆开理解2
“物质的量”描述的对象是微观粒子可以是:分子、原子、离子、原子团;还可以是:质子、中子、电子等
粒子必须十分明确,且用化学式表示判断下列说法是否正确(A)1摩尔氧(B)1摩尔氧原子(C)2摩尔分子氢(D)3摩尔水(E)0
5摩二氧化碳思考:错误,必须指明微粒的种类,是氧原子、氧分子还是氧离子正确1molO错误,2molH2正确3molH2O正确0
5molCO21mol到底有多大呢
•标准:每摩尔物质中含有6
02×1023个微粒以12g12C中所含的原子数目为标准的,也就是说,如果在一定量的粒子集体中所含有的粒子数与12g12C中所含的碳原子数目相同,则它的物质的量为1mol,而这个数值(粒子数)就叫阿伏加德罗常数(1)数值:阿伏加德罗常数,用NA表示
(2)规定:1mol任何粒子的粒子数叫做阿伏加德罗常数
(3)近似值:6
021023单位(mol-1)(4)物质的量、阿伏加德罗常数与粒子数(符号为N)之间的关系:n=NNA物质的量阿伏加德罗常数粒子数思考:2、1molC中约含有个碳原子3、0
3molH2SO4含有个硫酸分子4、1molNa2CO3中约含有_____molNa+、______molCO32-