第二节元素周期律第二节元素周期律((第第22课时课时))第二节:元素周期律(第1课时)小结1、随着原子序数的递增,元素原子的最外层电子排布呈现周期性变化
(由1-8)2、随着原子序数的递增,元素原子半径呈现周期性变化
3、着原子序数的递增,元素的化合价呈周期性变化(+1-+7,-4—-1)
4、元素的金属性,指元素的原子失去电子的能力;元素的非金属性,指元素的原子得到电子的能力
金属性强(弱)——单质与水反应或酸反应生成氢气容易(难),氢氧化物的碱性强(弱)
非金属性强(弱)——单质与氢气易(难)反应,生成的氢化物稳定(不稳定),氧化物的水化物酸性强(弱)
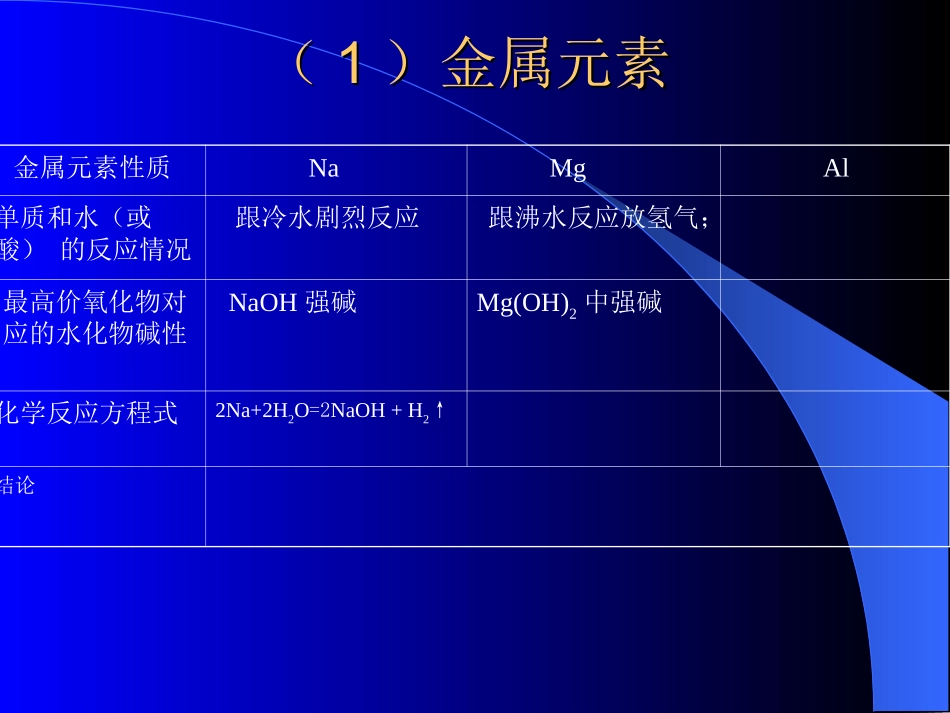
((11)金属元素)金属元素金属元素性质NaMgAl单质和水(或酸)的反应情况跟冷水剧烈反应跟沸水反应放氢气;最高价氧化物对应的水化物碱性NaOH强碱Mg(OH)2中强碱化学反应方程式2Na+2H2O=2NaOH+H2↑结论((11)金属元素)金属元素金属元素性质NaMgAl单质和水(或酸)的反应情况跟冷水剧烈反应跟沸水反应放氢气;最高价氧化物对应的水化物碱性NaOH强碱Mg(OH)2中强碱化学反应方程式2Na+2H2O=2NaOH+H2↑Mg+2H2O=Mg(OH)2+H2↑结论((11)金属元素)金属元素金属元素性质NaMgAl单质和水(或酸)的反应情况跟冷水剧烈反应跟沸水反应放氢气;跟酸剧烈反应放氢气跟酸较为迅速反应放出氢气最高价氧化物对应的水化物碱性NaOH强碱Mg(OH)2中强碱Al(OH)3两性氢氧化物化学反应方程式2Na+2H2O=2NaOH+H2↑Mg+2H2O=Mg(OH)2+H2↑结论((11)金属元素)金属元素金属元素性质NaMgAl单质和水(或酸)的反应情况跟冷水剧烈反应跟沸水反应放氢气;跟酸剧烈反应放氢气跟酸较为迅速反应放出氢气最高价氧化物对应的水化物碱性NaOH强碱Mg(OH)2