专题复习 物质构成的奥秘第一课时 化学用语 练习 找出下列符号中的错误,并讲出正确符号的意义
①N Mg②2+ S③2- ④ -2 S ⑤+1 ⑥+ Na ⑦1+NaNa 离子符号与化合价的比较 相同点① 元素符号相同② 数值与正负相同不同点① 书写位置不同② 数字与正、负号前后顺序不同③ 离子符号“ 1” 省略不写出 请你归纳出离子符号与化合价符号的书写有何不同
• ① 地壳中含量前四位的元素:• ② 生物细胞中含量前四位的元素:• ③ 空气中前二位的元素: 化学式的书写方法 化合物 金属元素左,非金属元素右 ,氧化物中氧在后,原子个数不能漏
单质 稀有气体和金属是由原子直接构成 , 及常温下为固态的大多数非金属 , 单质直接由元素符号来表示
如: He , Ne, Fe ,Cu , S , P 判断正误:下列化学式中书写正确的是 ( )A 氯化锌—— ZnCl B 氧化铝—— OAlC 氧化钠—— NaO D 硫酸镁—— MgSO4E 氦气———— He2化学式书写的判断 化学式表示的意义① 由分子构成的物质,其化学式意义(以 CO2为例):② 由原子构成的物质,其化学式的意义(以 Fe 为例): 化学方程式 1读
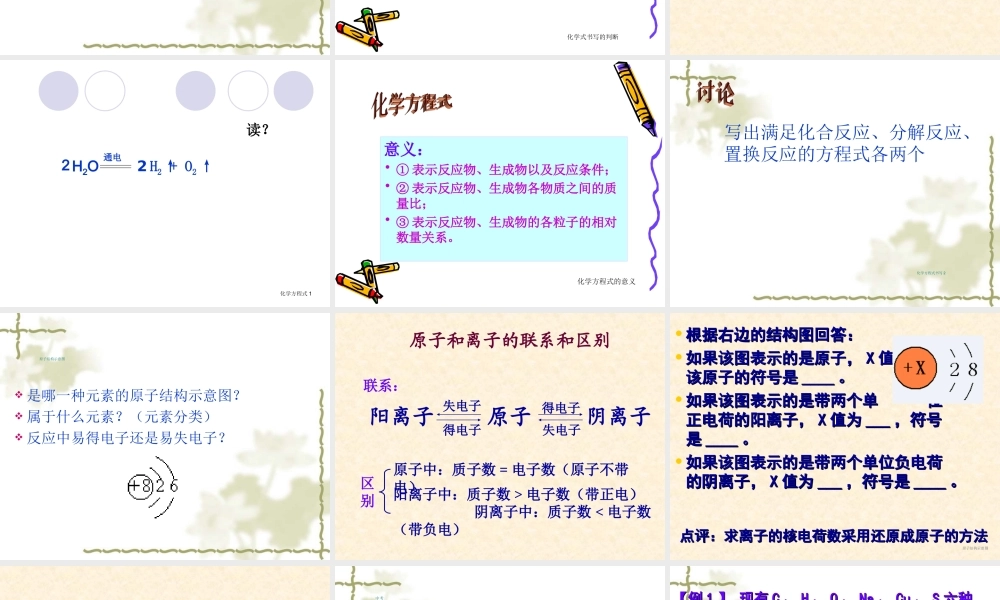
通电↑H2 + O2H2O2↑2 意义:• ① 表示反应物、生成物以及反应条件;• ② 表示反应物、生成物各物质之间的质量比;• ③ 表示反应物、生成物的各粒子的相对数量关系
化学方程式的意义 化学方程式书写 2写出满足化合反应、分解反应、置换反应的方程式各两个 原子结构示意图 是哪一种元素的原子结构示意图
属于什么元素
(元素分类) 反应中易得电子还是易失电子
原子阳离子阴离子失电子得电子失电子得电子原子中:质子数 = 电子数(原子不带电)阳离子中:质子数 > 电子数(带正电) 阴离子中:质子数 < 电子数(带负电)原子和离子的联系和区别