高三化学第一轮复习 电化学部分§1 原电池§2 化学电源§4 金属的电化学腐蚀与防护电化学基础§3 电解池知识结构1 、理解原电池和电解池的工作原理,能写出常见的简单电极反应和电池反应方程式
2 、了解常见的化学电源,认识化学能与电能相互转化的实际意义及其重要应用
3 、认识金属腐蚀的危害,理解金属发 生电 化学腐蚀的原因,能选用恰当的措施防 止铁、铝等金属腐蚀
《考试大纲》要求 电极名称和电极反应式 判断金属活动性 判断电极材料和电解质的种类 新型电池的电极反应及应用 ( 燃料电池) 有关电极产物的判断和计算历年高考常考知识点1
( 2014· 全国理综 II 化学卷, T12 )2013 年 3 月我国科学家报道了如图所示的水溶液锂离子电池体系
下列叙述错误的是A . a 为电池的正极B .电池充电反应为 LiMn2O4=Li1-xMn2O4+xLiC .放电时, a 极锂的化合价发生变化D .放电时,溶液中的 Li+ 从 b 向 a 迁移2 .( 2014· 全国理综 II 化学卷, T27 )( 3 ) PbO2 可由 PbO 与次氯酸钠溶液反应制得反应的离子方程式为 ; PbO2 也可以通过石墨为电极 Pb(NO3)2 和 Cu(NO3)2 的混合溶液为电解液电解制取
阳极发生的电极反应式为
阴极上观察到的现象是 ;若电解液中不加入 Cu(NO3)2 ,阴极发生的电极反应式为 ,这样做的主要缺点是
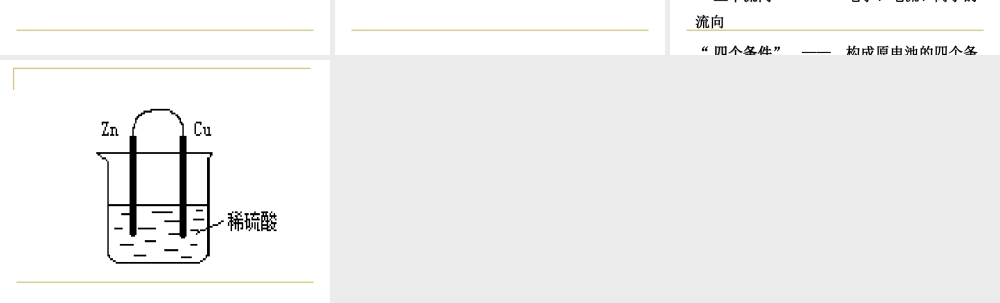
第一课时核心问题探究“ 一个概念一个概念” —— 原电池“ 两种电极两种电极” —— 正、负极判断及电极反应“ 三个流向三个流向” —— 电子、电流、离子的流向“ 四个条件四个条件” —— 构成原电池的四个条件