第二章 海水中的重要元素—钠和氯 2
1 氯气的性质 教学设计 一、教学目标 1.了解氯及其重要化合物的主要性质 2.认识燃烧现象的本质 3.了解次氯酸的性质及应用 二、教学重难点 1.教学重点 了解氯的化学性质;了解氯与碱的反应;掌握实验室制氯气的方法 2.教学难点 氯的化学性质;实验室制氯气的方法 三、教学过程 教学环节 教学内容 设计意图 1
新课导入 氯是一种重要的“成盐物质”
在自然界中除了以NaCl、MgCl2、CaCl2 等形式大量存在于海水中,还存在于陆地的盐湖和盐矿中
氯的单质氯气是一种重要的化工原料
大量用于制造盐酸、有机溶剂、农药、染料和药品等
18 世纪70 年代,瑞典化学家舍勒将软锰矿与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体
受当时流行学说的影响,舍勒未能确认这种气体
直到1810 年,英国化学家戴维才确认这种气体是一种新元素组成的单质——氯气
联系实际生活,情景带入 2
探索新知 【师】一.氯的结构 氯元素在自然界中以单质存在,主要以离子形式存在于海水和陆地的盐矿中
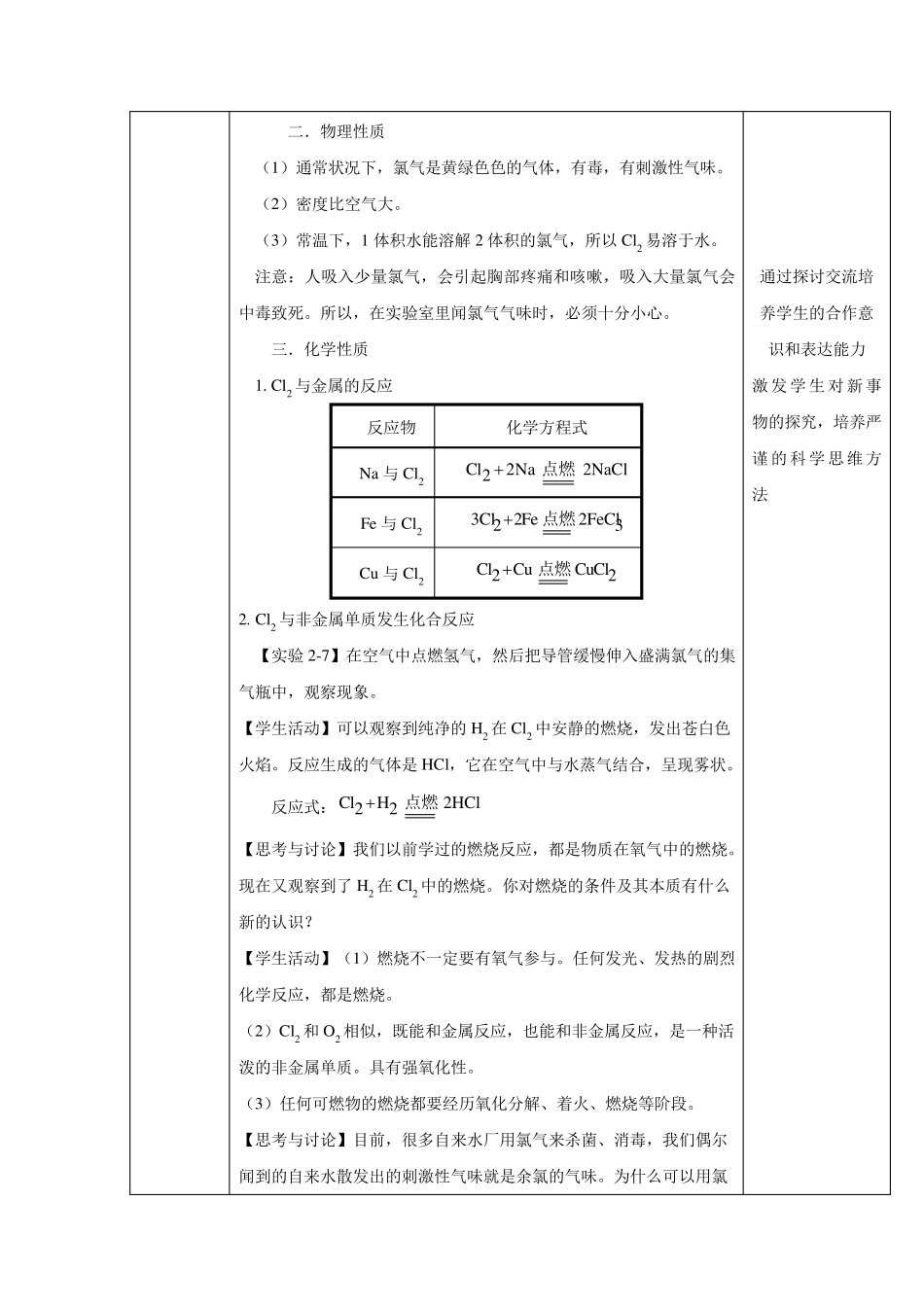
氯的原子结构示意图为,氯原子最外层有7 个电子,易 电子,达到8 个电子的稳定结构
故氯元素的非金属性很强,在化学反应中表现出很强的氧化性
二.物理性质 (1)通常状况下,氯气是黄绿色色的气体,有毒,有刺激性气味
(2)密度比空气大
(3)常温下,1 体积水能溶解2 体积的氯气,所以Cl2 易溶于水
注意:人吸入少量氯气,会引起胸部疼痛和咳嗽,吸入大量氯气会中毒致死
所以,在实验室里闻氯气气味时,必须十分小心
三.化学性质 1
Cl2 与金属的反应 反应物 化学方程式 Na 与Cl2 2NaCl 2Na2Cl点燃 Fe 与Cl2 32FeCl Fe223Cl点燃 Cu 与Cl2 2CuCl Cu 2Cl点燃 2
Cl2 与非金属单质发生化合反