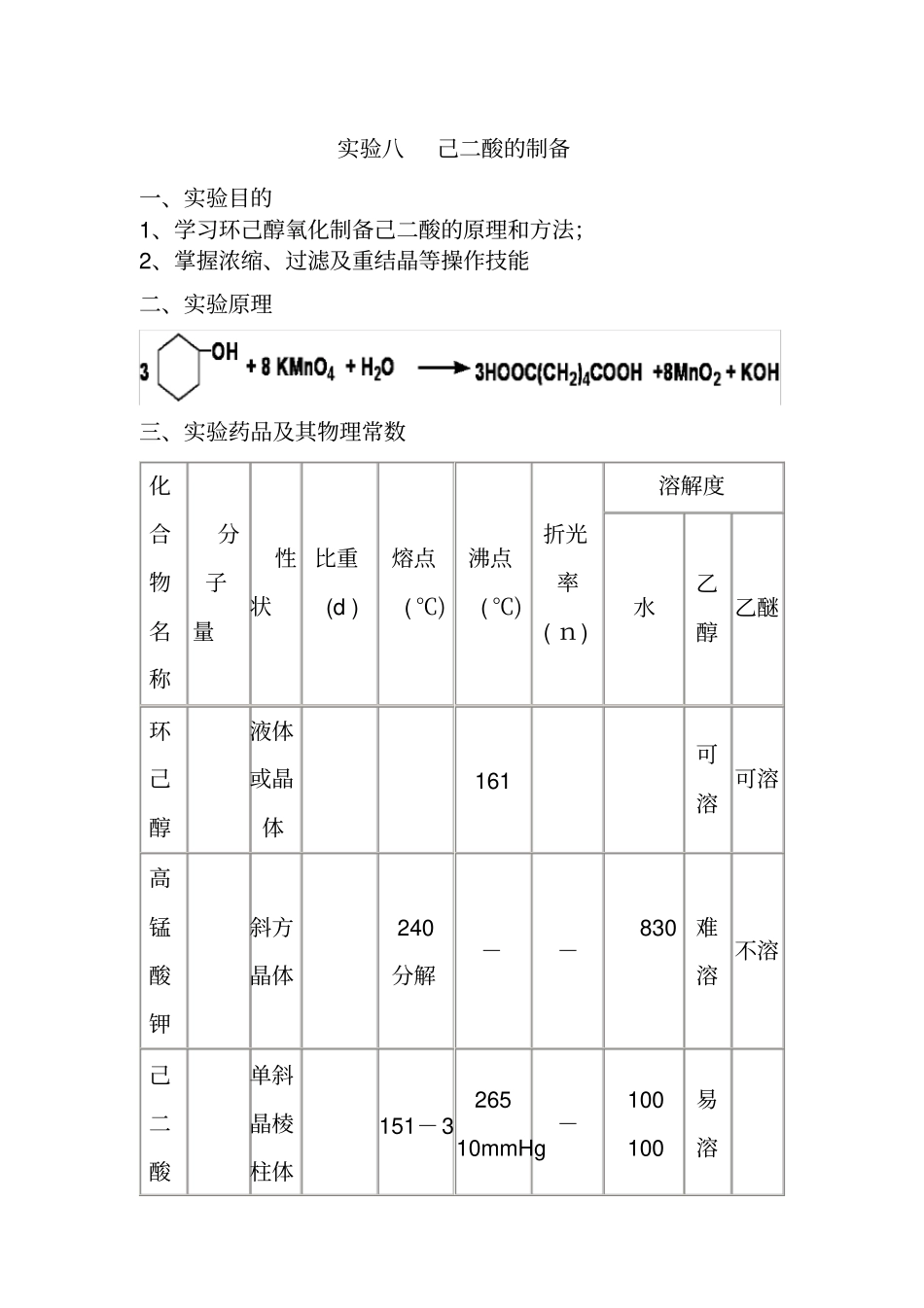
实验八己二酸的制备一、实验目的1、学习环己醇氧化制备己二酸的原理和方法;2、掌握浓缩、过滤及重结晶等操作技能二、实验原理三、实验药品及其物理常数化合物名称分子量性状比重(d )熔点( ℃)沸点( ℃)折光率( n)溶解度水乙醇乙醚环己醇液体或晶体161可溶可溶高锰酸钾斜方晶体240分解--830难溶不溶己二酸单斜晶棱柱体151-326510mmHg-100100易溶环己醇: 2g ;高锰酸钾6g ;氢氧化钠溶液 50ml ;亚硫酸氢钠;浓盐酸四、主要仪器和材料水浴锅三口烧瓶 (100 mL 、19#×3) 恒压滴液漏斗空心塞 (14#) 球形冷凝管 (19#) 螺帽接头 (19# ,2 只) 温度计(100℃) 布氏漏斗吸滤瓶烧杯冰 滤纸水泵等
氧化剂可用浓硝酸、碱性高锰酸钾或酸性高锰酸钾
本实验采用碱性高锰酸钾作氧化剂五、实验装置六、操作步骤(1)向 250ml 烧杯内加入50ml 氢氧化钠溶液,置于磁力搅拌上;(2)边搅拌边将6g 高锰酸钾溶解到氢氧化钠溶液中;(3)用滴管滴加环己醇到上述溶液中,维持反应物温度为 43~47 ℃
(4)当醇滴加完毕且反应混合物温度降低至43 ℃左右时,沸水浴将混合物加热,使二氧化锰凝聚
(5)在一张平整的滤纸上点一小滴混合物以试验反应是否完成,如果观察到试液的紫色存在,那么可以用少量固体亚硫酸氢钠来除掉过量的高锰酸钾
(6)趁热抽滤,滤渣二氧化锰用少量热水洗涤3 次( 每次 2 mL) ,每次尽量挤压掉滤渣中的水分;(7) 合并滤液和洗涤液,用4ml 浓盐酸酸化至;(8) 小心地加热蒸发使溶液的体积减少到10ml 左右,冷却,分离析出的己二酸
(9) 抽滤、洗涤、烘干、称重、计算产率
(10)测量产品的熔点和红外光谱,并与标准光谱比较
【操作要点及注意事项】要研细 , 以利于 KMnO4充分反应
滴加: 本实验为强烈放热反应,所