专题二十三 化学基本计算及常用的化学计算技巧 江苏省新海高级中学 袁武山【考纲要求】由于化学计算涉及的知识面广,对学生综合能力的考查最为明显,所以也是高考考查的热点
化学计算要掌握的技能和技巧如下:1
掌握有关化学量和化学式等基础知识的计算,并能熟练运用化学计算中的有关技能和技巧
掌握化学基本概念、基本理论及元素的单质和其重要的化合物、有机化学基础、化学实验等知识内容中,具有计算因素的各类问题的综合运用能力
从定量的角度上和在较高的深度上,来考查学生的思维品质,即思维的敏捷性、思维的严密性、思维的整体性和思维的创造性等
4.考查学生对相关学科知识的运用能力及将中学各科知识形成网络和体系的能力
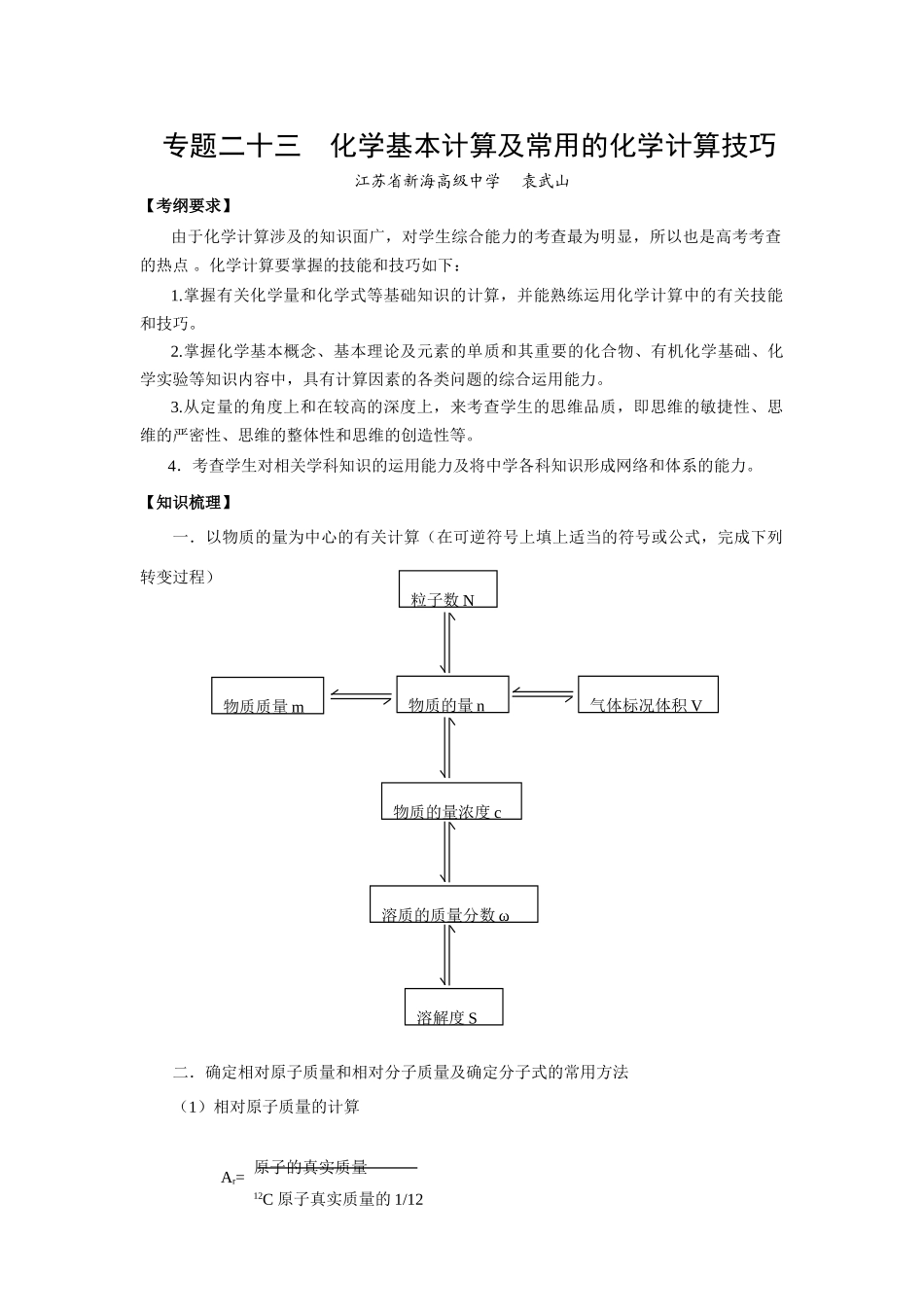
【知识梳理】一.以物质的量为中心的有关计算(在可逆符号上填上适当的符号或公式,完成下列转变过程)二.确定相对原子质量和相对分子质量及确定分子式的常用方法(1)相对原子质量的计算物质的量 n粒子数 N气体标况体积 V物质质量 m物质的量浓度 c溶质的质量分数 ω溶解度 SAr= 原子的真实质量12C 原子真实质量的 1/12①② 元素的相对原子质量与各同位素原子的相对原子质量及丰度的关系:____________________________________________________________③ 由化学式(AxBy)各元素的质量比(a:b)可得(2)相对分子质量的计算① 由分子式求相对分子质量② 由摩尔质量求相对分子质量(在数值上二者相等)Mr=M=m/n③ 对于气体还可以通过相对密度来求Mr=22
4ρ(ρ 为标况下气体的密度,单位为 g/L)M1=DM2(D 为两种气体的相对密度即:ρ1/ρ2=D)(3)分子式的确定常用方法:a、最简式法(通过相对分子质量)b、物质的量关系法(通过摩尔质量)c、化学方程式(通过质量守恒)d、通式法(对有机物而言)三.与溶解度有