第3课时化学平衡常数教学设计活动教学内容设计意图【情景导入】【教师活动】【学生活动】【投影】【教师活动】【学生活动】血液的pH保持在7
45是非常必要的,血液中存在以下平衡体系:,这一平衡体系对维持pH的变化范围起重要作用
不正确的呼吸可能导致血液中酸碱不平衡.太快或太深的呼吸会导致呼吸碱中毒,太慢或太浅的呼吸会导致呼吸酸中毒,那么我们应如何定量求得正常呼吸C02的范围
我们知道,一定条件下的可逆反应存在化学平衡状态
那么,当达到化学平衡状态时,究竟有多少反应物转化成了生成物,平衡体系中各物质的浓度之间是否有一定的关系
请大家完成第44页的“问题解决”
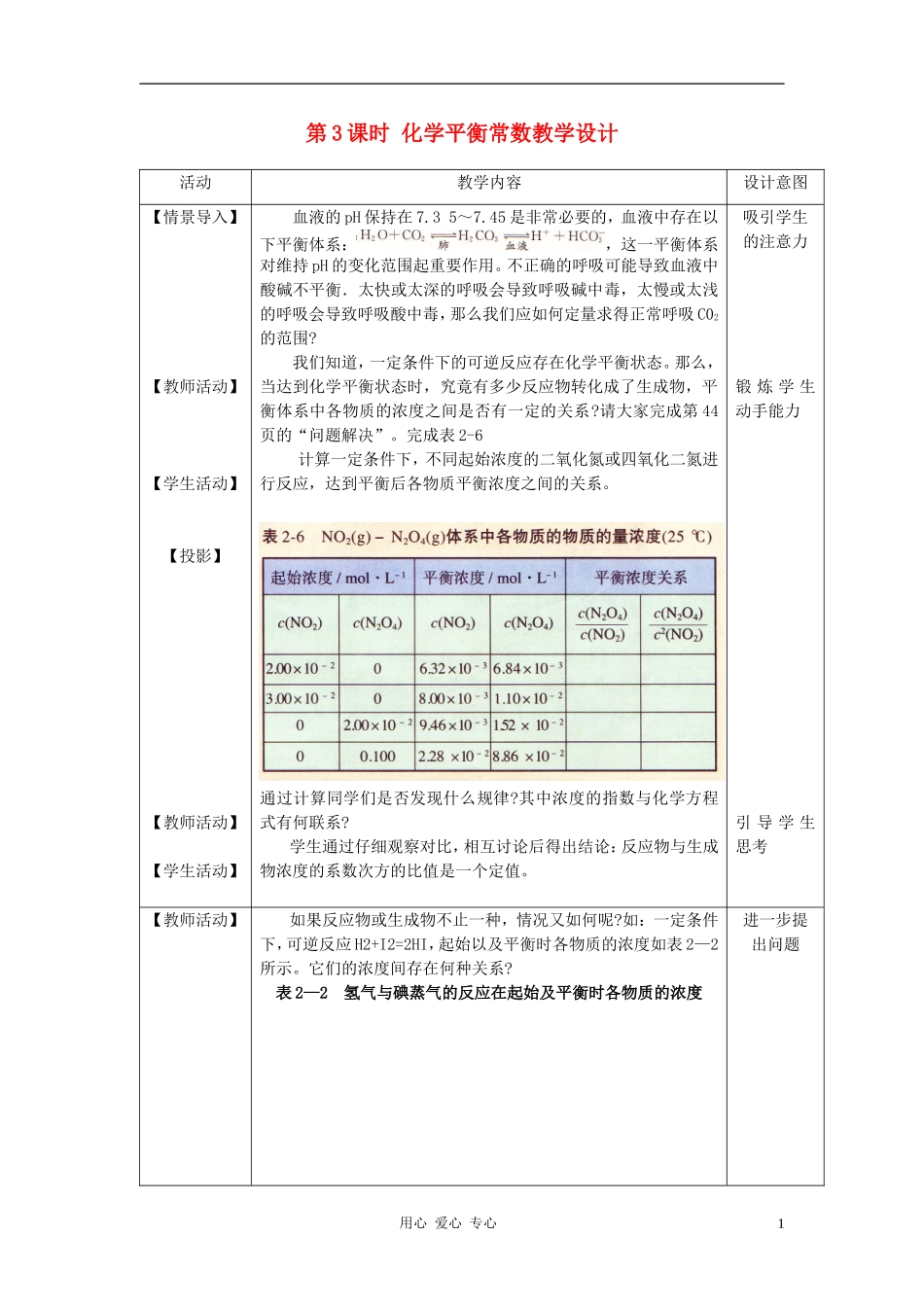
完成表2-6计算一定条件下,不同起始浓度的二氧化氮或四氧化二氮进行反应,达到平衡后各物质平衡浓度之间的关系
通过计算同学们是否发现什么规律
其中浓度的指数与化学方程式有何联系
学生通过仔细观察对比,相互讨论后得出结论:反应物与生成物浓度的系数次方的比值是一个定值
吸引学生的注意力锻炼学生动手能力引导学生思考【教师活动】如果反应物或生成物不止一种,情况又如何呢
如:一定条件下,可逆反应H2+I2=2HI,起始以及平衡时各物质的浓度如表2—2所示
它们的浓度间存在何种关系
表2—2氢气与碘蒸气的反应在起始及平衡时各物质的浓度进一步提出问题用心爱心专心1【学生活动】【教师活动】【学生活动】【板书】【教师活动】【学生活动】【师生活动】【板书】【投影】通过猜测并计算得出结论:是一个定值
引导学生阅读教材第45页有关化学平衡常数的定义,并找出关键词
认真阅读教材,纷纷找出一些关键词:“一定温度”、“无论起始浓度如何”等
一、化学平衡常数1、概念:在一定温度下,无论反应物的起始浓度如何,当一个可逆反应达到化学平衡状态时,生成物浓度系数次幂乘积与反应物浓度系数次幂乘积的比值是一个常数
2、表达式:对于可逆反应aA+Bb==cC+d