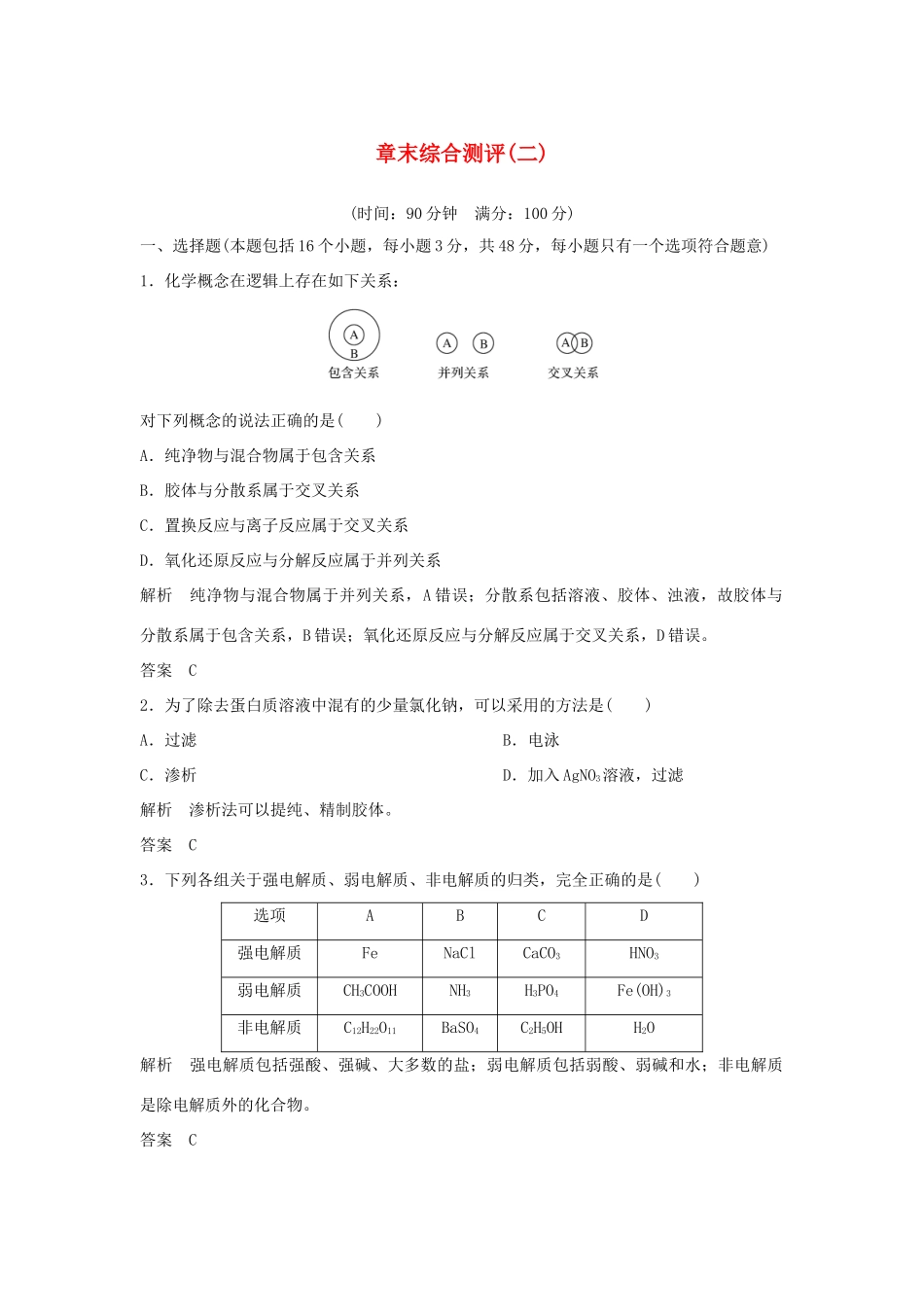
章末综合测评(二)(时间:90分钟满分:100分)一、选择题(本题包括16个小题,每小题3分,共48分,每小题只有一个选项符合题意)1.化学概念在逻辑上存在如下关系:对下列概念的说法正确的是()A.纯净物与混合物属于包含关系B.胶体与分散系属于交叉关系C.置换反应与离子反应属于交叉关系D.氧化还原反应与分解反应属于并列关系解析纯净物与混合物属于并列关系,A错误;分散系包括溶液、胶体、浊液,故胶体与分散系属于包含关系,B错误;氧化还原反应与分解反应属于交叉关系,D错误。答案C2.为了除去蛋白质溶液中混有的少量氯化钠,可以采用的方法是()A.过滤B.电泳C.渗析D.加入AgNO3溶液,过滤解析渗析法可以提纯、精制胶体。答案C3.下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是()选项ABCD强电解质FeNaClCaCO3HNO3弱电解质CH3COOHNH3H3PO4Fe(OH)3非电解质C12H22O11BaSO4C2H5OHH2O解析强电解质包括强酸、强碱、大多数的盐;弱电解质包括弱酸、弱碱和水;非电解质是除电解质外的化合物。答案C4.下面有关氧化还原反应的叙述正确的是()A.在反应中不一定所有元素的化合价都发生变化B.肯定有一种元素被氧化,另一种元素被还原C.非金属单质在反应中只作氧化剂D.金属原子失电子越多,其还原性越强解析氧化还原反应的宏观特征是元素化合价有升降,但不一定是所有元素化合价均有升降,故A正确;化合价变化的元素可以是不同种元素,也可以是同种元素,故B不正确;作为非金属在反应中一般作为氧化剂,但也有失电子的可能,故C不正确;金属具有还原性,还原性指失电子能力的强弱,而不是失电子数越多,还原性越强,故D不正确。答案A5.下列反应中,不是氧化还原反应的是()①H2+Cl2=====2HCl②Na2CO3+2HCl===2NaCl+H2O+CO2↑③2H2O=====2H2↑+O2↑④CuO+2HNO3===Cu(NO3)2+H2O⑤2HgO=====2Hg+O2↑A.②④B.①③C.①②③D.④⑤解析氧化还原反应的特征是元素化合价有升降。答案A6.长期放置在空气中会变质并发生氧化还原反应的是()A.生石灰B.白磷C.无水硫酸铜D.十水硫酸钠解析B项中白磷在空气中因被氧化而自燃。答案B7.一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是()A.NaCl是非电解质B.NaCl溶液是电解质C.NaCl在水溶液中电离出可以自由移动的离子D.NaCl溶液中水电离出大量的离子解析NaCl是电解质,但NaCl固体不导电;NaCl在水溶液中能电离出大量的可自由移动的钠离子和氯离子,使溶液能导电。答案C8.在pH=1的无色透明的溶液中能大量共存的离子组是()A.Al3+、Cu2+、NOB.Na+、SO、S2-C.Mg2+、NH、Cl-D.K+、HCO、Cl-解析pH=1则溶液呈酸性,且溶液无色。A项Cu2+显蓝色;B项S2-与氢离子反应;D项HCO与氢离子反应。答案C9.某研究性学习小组的同学做了一个趣味实验:将一只鸡蛋放入食醋中,过一会儿发现蛋壳表面附有气泡,第二天发现蛋壳变软了。你认为鸡蛋壳与食醋发生反应的离子方程式正确的是()A.CO+2H+===H2O+CO2↑B.CaCO3+2H+===Ca2++H2O+CO2↑C.CaCO3+2CH3COOH===Ca2++2CH3COO-+H2O+CO2↑D.CO+2CH3COOH===2CH3COO-+H2O+CO2↑解析蛋壳的主要成分是难溶物CaCO3,食醋的主要成分是弱酸CH3COOH,生成物醋酸钙易溶于水。答案C10.在一定条件下,氯酸钾和碘按下式发生反应:2KClO3+I2===2KIO3+Cl2,由此推断下列相应的结论不正确的是()A.该反应属置换反应B.还原性:I2>Cl2C.氧化性:I2>Cl2D.氧化性:KClO3>KIO3解析反应中有单质参加且有单质生成,是置换反应;反应中还原剂I2的还原性大于还原产物Cl2。答案C11.在2H2S+SO2===3S↓+2H2O的反应中,还原产物和氧化产物的质量比是()A.1∶1B.2∶1C.1∶2D.2∶3解析根据反应化合价可判断硫既是氧化产物又是还原产物。答案C12.下列关于Fe(OH)3胶体的叙述中,正确的是()A.制备Fe(OH)3胶体的化学方程式是FeCl3+3H2O=====Fe(OH)3↓+3HClB.在制备Fe(OH)3胶体的实验中,加热煮沸时间越长,越有利于胶体的生成C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同D.Fe(OH)3胶...