第二章第1节化学键与化学反应(1)【教材分析】在前边原子结构和元素周期律知识的基础上,引导学生进一步探索原子是如何结合成为分子的
通过对化学键概念的建立,使学生在原子、分子的水平来认识物质的构成和化学反应
人们研究化学反应,有两个主要的目的:一个是研究物质的组成(或得到新的物质),二是研究物质变化时伴随的能量改变
两者是紧密联系的
新教材就突出了这一点,把化学变化和能量变化放到一起来讲,使学生懂得在物质发生化学变化的同时也伴随有能量的变化,从两个视角来关注化学反应,从而为认识化学反应和应用化学反应奠定基础
【教学过程】教学目标1
了解化学键的含义,认识共价键的形成过程与形成条件2
了解化学键类型与物质构成的关系,以某一化学反应为背景,学习化学键,从而更好的认识物质构成和化学反应的本质教学重点教学难点化学键、共价键的含义和对化学反应实质的理解高考考点化学键、共价键课型新授课教具多媒体教法两先两后一小结教学过程教学环节教师活动学生活动设计意图引入课题自学习化学以来,已接触过许多化学反应,而且在分析这些化学反应时,主要是考虑参与反应的物质通过反应生成了什么物质
其实在化学反应中,不仅有物质变化,还伴随能量变化
利用化学反应,有时为了制取物质,有时利用释放能量
本节课我们将要探究化学键与化学反应中物质的变化
聆听、思考;明确本节课学习目标---化学键与化学反应交流
研讨【板书】第1节化学键与化学反应展示化学反应的应用、木炭燃烧、水在通电条件下分解等图片,引领学生观察,并思考问题
化学反应中为什么会发生物质变化
化学反应中的最小微粒是什么
水为什么要通电才会分解
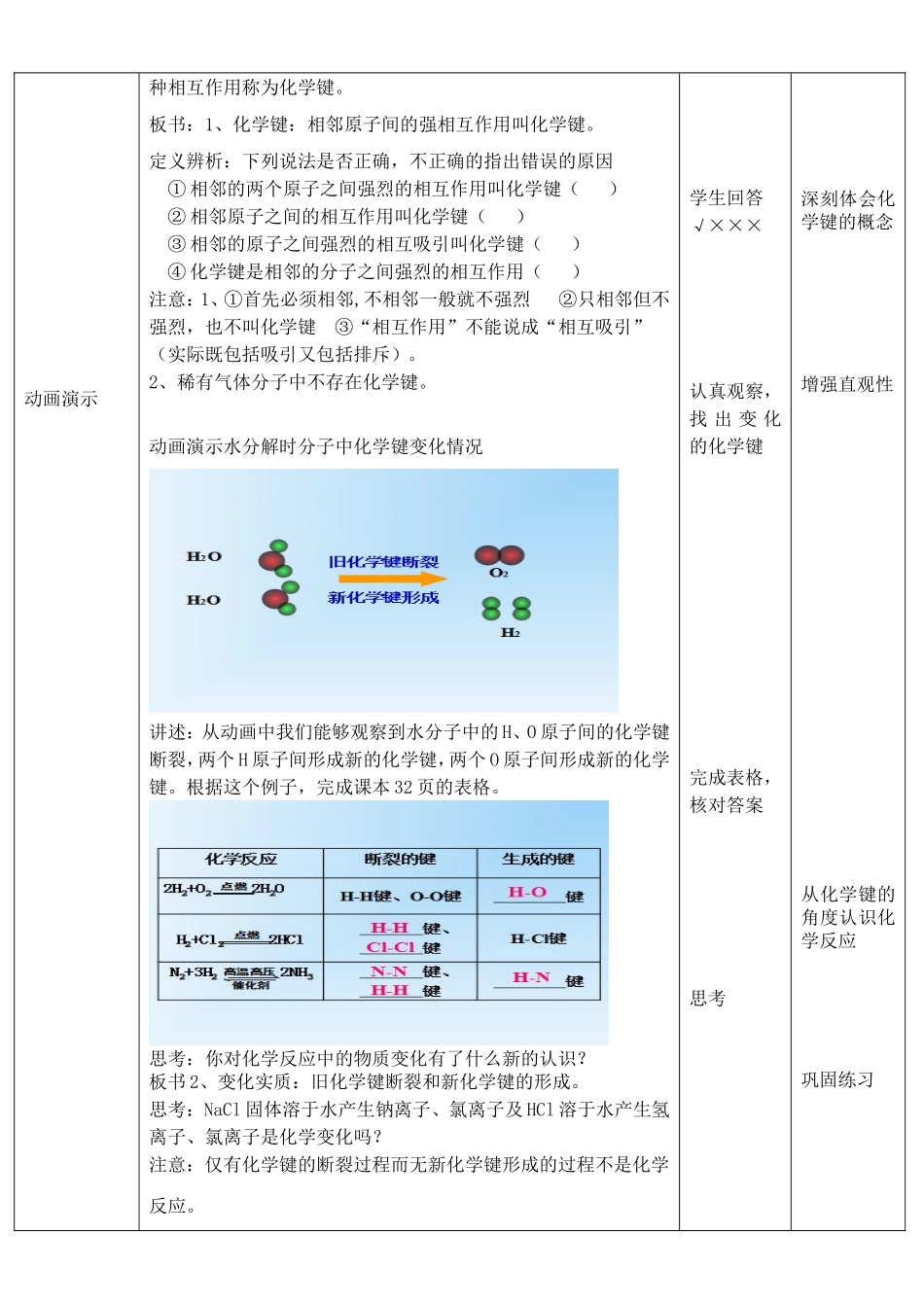
讲解:水分子是由两个氢原子和一个氧原子构成的,氢原子和氧原子之间存在着很强的相互作用,要破坏这种相互作用就需要消耗能量,通电正是为了提供使水分解所需要的能量
我们就把这观看图片、思考;原子重新组合;分子思考通